
(11分)A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如下图所示(部分产物已略去)

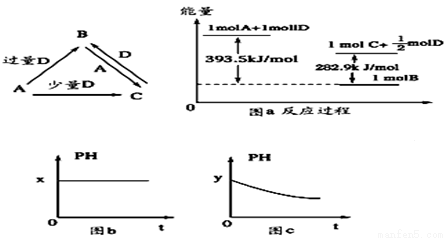
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为____________。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为________________。
②反应B+A→C的离子方程式为____________________________。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)
①若图b符合事实,则D为________(填化学式),此时图b中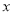 ________7(填“﹥”“﹤”“=”)。若图c符合事实,则其pH变化的原因是_____________(用离子方程式表示)。
________7(填“﹥”“﹤”“=”)。若图c符合事实,则其pH变化的原因是_____________(用离子方程式表示)。
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出1molA和D反应生成C的反应热为ΔH=________________。
(1)3Fe2++4H++NO3ˉ=3Fe3++NO↑2H2O (2分)
(2)Al(OH)3 (1分) Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分)
(3)CO2 (1分) > (1分) 2HSO3ˉ+O2=2SO42-+2H+(2分) (4) △H=-110.6 kJ/mol (2分)
【解析】
试题分析:(1)A为金属单质,D是某强酸的稀溶液,由图可知,A为Fe,C为硝酸亚铁,B为硝酸铁,D为硝酸,则反应C+D→B的离子方程式为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O;
(2)A、B为盐,D为强碱,A的水溶液显酸性,则A可为AlCl3,D可为NaOH,C为Al(OH)3,B为NaAlO2,则
①由上述分析可知,C为Al(OH)3;
②反应B+A→C的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)A为强碱,D为气态氧化物,由转化图可知,A可为NaOH,D为CO2或SO2,B为NaHCO3或NaHSO3,常温时将B的水溶液露置于空气中,若为b,则碳酸氢钠符合,若为c则亚硫酸氢钠符合,则
①若图b符合事实,则D为CO2;因碳酸氢钠水解显碱性,则图b中x>7;
②若图c符合事实,亚硫酸氢钠易被氧化生成硫酸氢钠,酸性增强,离子反应为2HSO3-+O2=2H++2SO42-;
(4)A为非金属单质,D是空气的主要成分之一,则A为C,D为O2,C为CO,由图可知,1molA和D反应生成C放出热量为393.5kJ-282.9kJ=110.6kJ,则A+D→C的热化学方程式为C(s)+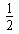 O2(g)=CO(g)△H=-110.6 kJ/mol。
O2(g)=CO(g)△H=-110.6 kJ/mol。
考点:考查无机物的推断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年云南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
某溶液中含有NH4+、Mg2+、Fe2+、Al3+和SO42—五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有
A.4种 B.3种 C.2种 D.1种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期第二次模考试化学试卷(解析版) 题型:选择题
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将8 g三氧化硫溶于水并配成1 L溶液
D.将0.1 mol氧化钠溶于水并配成1 L溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是:
A、过量的铁在氯气中燃烧可生成氯化亚铁
B、向Fe(NO3)2溶液加入盐酸,由于酸性增强抑制Fe2+的水解,使c(Fe2+)增大
C、Fe和Fe2O3的混合物溶于盐酸中,再加入KSCN溶液,溶液一定变为血红色
D、把一定量的铁和铜的混和粉未投入到FeCl3溶液中,不可能出现只有铁剩余没有铜剩余的情况
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三上学期期中化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.在纯水中加入能水解的盐一定促进水的电离
B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C.加热CH3COONa溶液,溶液中  的值将减小
的值将减小
D.常温下醋酸分子不可能存在于pH>7的碱性溶液中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省赣州市十二县高三上学期期中化学试卷(解析版) 题型:选择题
A、B、C、D、E五种短周期元素原子序数依次增大,A原子为半径最小的原子,C原子最外层电子数与A、B原子最外层电子数之和相等,D原子和B原子最外层电子数的和为C原子最外层电子数的2倍,D原子的最外层电子数为电子层数的3倍,A、E同一主族。下列说法正确的是
A.原子半径大小顺序为:E>D>C>B>A
B.A、B、C、D四种元素都属于非金属元素,它们之间只能形成共价化合物
C.B、C、D、E四种元素与A 元素形成的最简单化合物的沸点依次升高
D.D与A、E均可形成具有强氧化性的化合物,可用于城市自来水的杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省赣州市十二县高三上学期期中化学试卷(解析版) 题型:选择题
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol?L-1和1.5mol?L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是
A.反应后溶液中Fe3+物质的量为0.8 mol
B.反应后产生13.44 L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol
D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三上学期期中化学试卷(解析版) 题型:选择题
下列各项中离子方程式的书写与反应物的用量无关的是
A.AlCl3溶液与稀氨水 B.FeBr2溶液与Cl2
C.CO2与Na2SiO3溶液 D.澄清石灰水与Ca(HCO3)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com