
【题目】【化学——选修3:物质结构与性质】
A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。请回答下列问题:
(1)当n=2时,AB2属于__________分子(填“极性”或“非极性”),分子中有__________个δ键、__________个π键。A6H6分子中A原子的杂化轨道类型是__________杂化。
(2)当n=3时,A与B形成的晶体属于__________晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是__________(用元素符号表示).
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为____________________。
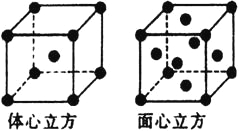
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为__________。
【答案】(1)非极性 2 2 sp2(2)原子(3)P>S>Si (4)1s22s22p63s23p63d6或[Ar]3d6(5)1∶2
【解析】
试题分析:A、B、C、D为前四周期元素,A元素的原子价电子排布为ns2np2,则A为ⅣA族元素,B元素原子的最外层电子数是其电子层数的3倍,最外层电子数不超过8个,B为氧元素,C元素原子的M能层的p能级有3个未成对电子,C为P元素,D元素原子核外的M能层中只有2对成对电子,则D是S元素。
(1)当n=2时,A是C元素,则AB2是CO2,二氧化碳是直线型结构,正负电荷重心重合,所以是非极性分子;CO2的结构式为O=C=0,分子中有2个δ键、2个π键。A6H6分子是C6H6,苯分子中C原子的杂化轨道类型是sp2杂化
(2)当n=3时,A是Si元素,硅和氧形成的晶体是二氧化硅晶体,二氧化硅晶体是由原子构成的,属于原子晶体。
(3)若A元素的原子价电子排布为3s23p2,则A是Si元素,同一周期中,原子的电负性随着原子序数的增大而呈增大趋势,但第VA族元素大于第VIA族元素,所以A、C、D三种元素的第一电离能由大到小的顺序P>S>Si。
(4)钴离子的化合价是+3价,钴离子核外有24个电子,其基态时核外电子排布式为1s22s22p63s23p63d6。
(5)根据均摊法计算,体心立方晶胞中铁原子个数为8×1/8+1=2,面心立方晶胞中铁原子个数为8×1/8+6×1/2=4,则实际含有的Fe原子个数之比为2:4=1:2.


科目:高中化学 来源: 题型:
【题目】已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知1mol单质碳完全燃烧放出热量为Y kJ,则1molC与O2反应生成CO的热量变化为
A.放出Y kJ B.放出(5X-5Y) kJ
C.放出(10X-Y) kJ D.吸收(10X-Y) kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修2:化学与技术]
软锰矿(主要成分为MnO2)可用于制备锰及其化合物。
(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为_______________。
(2)现代冶炼金属锰的一种工艺流程如下图所示:
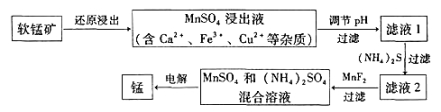
下表为t℃时,有关物质的pKsp(注:pKsp =-lgKsp)。
物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4 ![]() 12MnSO4+6CO2↑+18H2O
12MnSO4+6CO2↑+18H2O
①该反应中,还原剂为_______。写出一种能提高还原浸出速率的措施:_______。
②滤液1的pH_______(填“大于”、“小于”或“等于”)MnSO4浸出液的pH。
③加入MnF2的主要目的是除去 (填Ca2+、Fe3+或Cu2+)。
(3)由MnSO4制取MnCO3:往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为____________;若往MnSO4溶液中加入(NH4)2CO3溶液,还会产生Mn(OH)2,可能的原因是:MnCO3(s)+2OH-(aq)![]() Mn(OH)2(s)+CO32-(aq),t ℃时,计算该反应的平衡常数K= (填数值)。
Mn(OH)2(s)+CO32-(aq),t ℃时,计算该反应的平衡常数K= (填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)与NH3互为等电子体的分子、离子有________、________(各举一例)。
(2)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1 mol CN-中含有的π键的数目为________;若此离子与[Cu(H2O)4]2+结构相似,则此离子的空间构型为 。
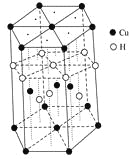
(3)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为________。
(4) 甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O-C-H键角________(填“大于”、“等于”或“小于”)甲醛分子内的O-C-H键角;甲醇易溶于水的原因是 。
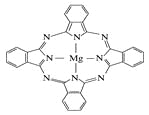
(5) 金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如图所示,其中N原子的杂化方式为 ,在如图的方框内请在图中用箭头表示出配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】含氮化合物在生活中应用十分广泛。神州飞船外壳使用了氮化硅新型陶瓷结构材料,该材料硬度大、耐磨损。可用石英与焦炭在1400~1450℃的氮气气氛下合成氮化硅,同时生成一种与氮气结构相似的气态分子。
(1)写出上述反应的化学方程式____________________________________。反应原料中涉及的元素电负性由大到小的排列顺序为________________________________。
(2)基态氮原子中的原子轨道形状有 _______________种。
(3)某同学画出了硅原子基态的核外电子排布图如下图,该电子排布违背了 原理。
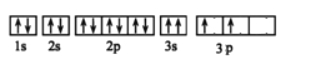
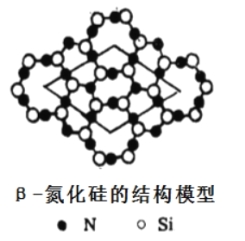
(4)氮化硅有多种型体,其中β-氮化硅层状结构模型如图,以图中所示的平行四边形为基本重复单元无限伸展,则该基本单元中含氮原子______个,硅原子______个。
(5)含氮的有机化合物氨基乙酸H2NCH2COOH中的碳 原子杂化方式有____________,σ与π键的个数比为_______________。
(6)氨分子是一种常见的配体。Cu2+离子在水溶液中以 [Cu (H2O)4]2+形式存在,向含Cu 2+离子的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+离子,其原因是 。某配合物的化学式为 CoCl3·4NH3, 内界为正八面体构型配离子。0.1 mol该化合物溶于水中,加入过量 AgNO3,有14.35g 白色沉淀生成。则它的中心离子价电子排布式为____________,內界可能的结构有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来各国都在寻找对环境无害而作用快速的消毒剂,其中二氧化氯(ClO2)是目前国际上倍受瞩目的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某兴趣小组的学生设计了如下模拟装置来制取、收集ClO2并测定其质量。
查阅资料:ClO2是一种黄红色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,温度过高可能引起爆炸,易溶于水,易与碱液反应。


实验Ⅰ:制取并收集ClO2,如图1装置所示。
(1)装置A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式__________。
(2)装置A必须添加温度控制装置,其温度要保持在60~80℃之间,控制温度的目的是__________。装置B也必须添加温度控制装置,应该是__________(填“冰水浴”或“沸水浴”或“60℃的热水浴”)装置。
实验Ⅱ:测定ClO2质量,如图2装置所示。过程如下:
在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;按照图2组装好仪器;在玻璃液封管中加入水,浸没导管口;将生成的ClO2气体由导管通入锥形瓶的溶液中充分吸收后,把玻璃液封管中的水封液倒入锥形瓶中,再向锥形瓶中加入几滴淀粉溶液:用cmol/L硫代硫酸钠标准液滴定锥形瓶中的液体,共用去VmL硫代硫酸钠溶液(己知:I2+2S2O32-=2I-+S4O62-)。
(3)装置中玻璃液封管的作用是____________________。
(4)滴定终点的现象是____________________。
(5)测得通入ClO2的质量m(ClO2)=__________g(用整理过的含c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
I.已知: ① 4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
②H2(g)+Cl2(g)=2HCl(g)△H=-184kJ/mol
由知断开1mol H-H键所需能量为436kJ;断开1molO=O键所需能量为496kJ;断开1molCl-Cl键所需能量为243KJ。则
(1)H2与O2反应生成气态水的热化学方程式是
(2)断开1molH-O键所需能量为 kJ。
Ⅱ.已知: CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.2kJmol-1 ①
CH4(g)+CO2(g)═2CO(g)+2H2(g) △H=+247.4kJmol-1 ②
又知CH4的燃烧热为890.3kJ/mol。
(1)利用上述已知条件写出甲烷完全燃烧的热化学方程式: 。
(2)以甲烷为原料制取氢气是工业上常用的制氢方法,CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为________________________________。
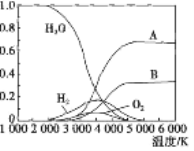
(3)高温下H2O可分解生成分子或原子。高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中B表示的微粒是_______(填名称),等质量的A、H2化学能较低的物质是_______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇可以补充和部分替代石油燃料,缓解能源紧张。利用CO可以合成甲醇。
(1)已知:CO(g)+![]() O(g)=CO2(g) △H1=-283.0kJ·mol-1
O(g)=CO2(g) △H1=-283.0kJ·mol-1
H2(g)+ ![]() O2(g)=H2O(l) △H2=-285.8kJ·mol-1
O2(g)=H2O(l) △H2=-285.8kJ·mol-1
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
则CO(g)+2H2(g)=CH3OH(g) △H=__________kJ·mol-1
(2)甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示平均反应速率v(H2)=____________________。
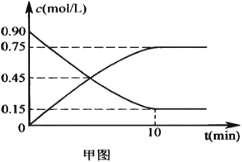
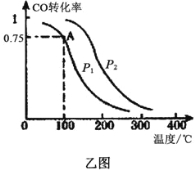
(3)一定条件下,在容积为VL的密闭容器中充入amolCO与2amolH2合成甲醇,平衡转化率与温度、压强的关系如乙图所示。
①P1__________P2(填“>”、“<”或“=”)
②该甲醇合成反应在A点的平衡常数K=__________(用a和V表示)
③下列措施中能够同时满足增大反应速率和提高CO转化率的是__________。(填写相应字母)
A.使用高效催化剂B.降低反应温度
C.增大体系压强D.不断将CH3OH从反应混合物中分离出来
E.向体系中再充入amolCO与2amolH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近研究用生物质原料合成高分子材料PET的流程如下:
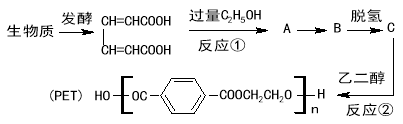
已知下列两个反应:
![]()
![]()
请回答下列问题:
(1)反应①属于 反应。
(2)PET的中文名称是 。
(3)有机物A、B的结构简式分别是 、 。
(4)写出反应②的化学方程式 。
(5)在有机物A的同分异构体F溶液中滴加氯化铁溶液显紫色。F的苯环上有四个取代基且一氯代物有只有一种,0.1molF 跟足量的金属钠反应,生成0.15mol氢气,F的核磁共振氢谱有4个吸收峰。试写出满足上述条件F的结构简式 (任写一种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com