
| m |
| M |
| V |
| Vm |
| N |
| NA |
| m |
| M |
| m |
| M |
| N |
| NA |
| 22.4L |
| 22.4L/mol |
| 9g |
| 18g/mol |
| 16g |
| 16g/mol |
| mg |
| 17g/mol |
| 17a |
| 4m |
| 2mg |
| 34g/mol |
| m |
| 17 |
| a |
| 4 |
| a |
| 4 |


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
 某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:
某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:Z>W>Y |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物为两性 |
| D、XW2是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、微粒
| ||
| B、漏斗、蒸馏烧瓶、分液漏斗、滴定管等仪器用于物质分离 | ||
| C、非金属氧化物一定属于非电解质 | ||
| D、在熔化状态下能导电的化合物为离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 分类标准 | 碱性氧化物 | 强电解质 | 含氧酸 | 非电解质 |
| 属于该类的物质 | ① | NaOH | ② | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
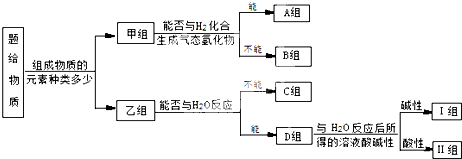
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④ |
| C、①③④⑤ | D、①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com