
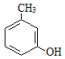
 +CH3COCH2COOC2H5$→_{10℃搅拌12h}^{浓硫酸}$
+CH3COCH2COOC2H5$→_{10℃搅拌12h}^{浓硫酸}$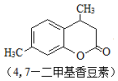 +C2H5OH+H2O
+C2H5OH+H2O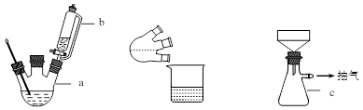
分析 (1)根据实验的需要结合大气压强原理来回答,装置b中将活塞上下部分连通,能平衡上下气压,使漏斗中液体顺利流下;
(2)根据装置构造和作用可得;
(3)浓硫酸具有强氧化性和脱水性,温度高能使有机物氧化和脱水碳化;
(4)反应需要搅拌12h,使反应物充分接触反应,提高反应产率;
(5)已知间甲苯酚30mL(0.29mol)、乙酰乙酸乙酯26.4mL (0.21mol),若完全反应间甲苯酚过量,按照乙酰乙酸乙酯计算求出理论产量,再求出产率.
解答 解:(1)装置中装置b中将活塞上下部分连通具有平衡气压的作用,使漏斗中间甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物顺利流下;
故答案为:平衡上下气压,使漏斗中液体顺利流下;
(2)装置从为抽滤瓶,与过滤相比,抽滤的优点是加快过滤速率;
故答案为:抽滤瓶;加快过滤速率;
(3)浓硫酸具有强氧化性和脱水性,反应温度高浓硫酸能使有机物氧化和脱水碳化,发生副反应,所以浓H2SO4需要冷却至0℃以下;
故答案为:防止浓H2SO4将有机物氧化或炭化;
(4)不断的搅拌反应混合物,可以使反应物充分接触反应,从而提高反应产率;
故答案为:使反应物充分接触反应,提高反应产率;
(5)已知间甲苯酚30mL(0.29mol)、乙酰乙酸乙酯26.4mL(0.21mol),若完全反应间甲苯酚过量,按照乙酰乙酸乙酯计算理论产量为0.21mol×176g/mol=36.96g,则产率为$\frac{33.0}{36.96}$×100%≈89.3%,
故答案为:89.3%.
点评 本题考查了有机物的制备实验,侧重于实验仪器、实验操作、产率的计算的考查,题目难度中等,考查了学生的实验探究能力.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:选择题
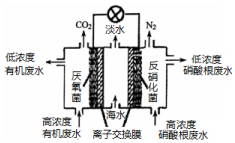
| A. | 该电池能在高温下工作 | |
| B. | 该电池工作时,中间室中的Cl-移向右室 | |
| C. | 正极上发生的电极反应:2NO3-+6H2O+10e-═N2↑+12OH- | |
| D. | 若有机废水中有机物用C6H12O6表示,每消耗1 mol C6H12O6转移4 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度升高,反应速率增大,产率增大 | |
| B. | 增大反应物H2的浓度,HI%增大 | |
| C. | 增大压强,浓度增大,平衡不移动 | |
| D. | 使用催化剂,反应速率增大,I2的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol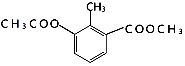 能与4molNaOH充分反应 能与4molNaOH充分反应 | |
| B. | 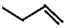 系统命名法为3-丁烯 系统命名法为3-丁烯 | |
| C. | 1mol 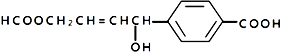 可以与4molH2发生加成 可以与4molH2发生加成 | |
| D. | 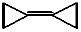 的碳原子都在一个平面内,且它的二氯代物为3种 的碳原子都在一个平面内,且它的二氯代物为3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
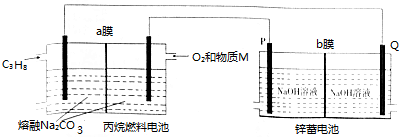
| A. | 物质M为CO2 | |
| B. | 燃料电池消耗1mo1 O2时,理论上有4 mol OH-透过b膜向P电极移动 | |
| C. | a膜、b膜均适宜选择阴离子交换膜 | |
| D. | 该装置中,锌蓄电池的正极反应式为Zn+2OH--2e-═ZnO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32gCu在足量O2或硫蒸气中完全燃烧失去的电子数均为NA | |
| B. | 4g甲烷和8g甲醇含有的氢原子数均为NA | |
| C. | 标准状况下,5.6L乙烷中含有的共价键数目为1.5NA | |
| D. | 一定条件下,32gSO2与足量O2反应,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
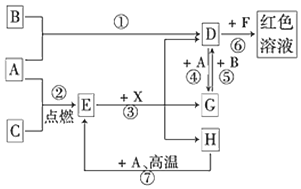
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
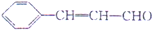 ),杏仁含苯甲醛(
),杏仁含苯甲醛(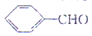 ).下列说法错误的是( )
).下列说法错误的是( )| A. | 肉桂醛和苯甲醛互为同系物 | |
| B. | 肉桂醛能发生加成反应、取代反应和加聚反应 | |
| C. | 可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团 | |
| D. | 1mol肉桂醛分子在一定条件下最多与5mol氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C7H12O4,4种 | B. | C7H12O4,6种 | C. | C7H14O2,8 种 | D. | C7H14O2,10种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com