
下列反应中,不是氧化还原反应的是 ( )
①H2+Cl2 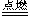 2HCl ②Na2CO3+2HCl==2NaCl+H2O+CO2↑ ③2H2O
2HCl ②Na2CO3+2HCl==2NaCl+H2O+CO2↑ ③2H2O  2H2↑+O2↑
2H2↑+O2↑
④CuO+2HNO3==Cu(NO3)2+H2O ⑤2HgO  2Hg+O2↑
2Hg+O2↑
A. ②④ B. ①③⑤ C. ①②③④ D ②③⑤
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
V L Fe2(SO4)3溶液中含有a g SO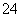 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
A.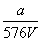 mol·L-1 B.
mol·L-1 B.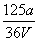 mol·L-1
mol·L-1
C.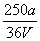 mol·L-1 D.
mol·L-1 D.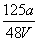 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO·Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
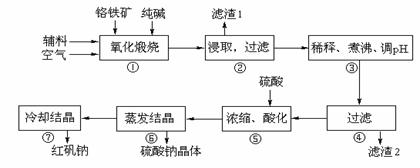
①中涉及的主要反应有:
主反应:4FeO·Cr2O3+8Na2CO3+7O2  8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3 Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3 2NaAlO2+CO
2NaAlO2+CO 2↑
2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
试回答下列问题:
⑴“①”中反应是在回转窑中进行 ,反应时需不断搅拌,其作用是
,反应时需不断搅拌,其作用是
⑵ “③”中调节pH至4.7,目的是 。
⑶ “⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式: 。
( 4)称取重铬酸钠试样2.5000 g配成250 mL溶液,取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放
4)称取重铬酸钠试样2.5000 g配成250 mL溶液,取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放 于暗处5 min,然后加入100 mL水,加入3 mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
于暗处5 min,然后加入100 mL水,加入3 mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①判断达到滴定终点的依据是:____________________________________;
②若实验中共用去Na2S2O3标准溶液40.00 mL,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在热的稀硫酸溶液中溶解了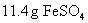 .当加入
.当加入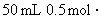
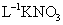 溶液后,使其中的
溶液后,使其中的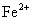 全部转化成
全部转化成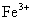 ,
,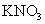 也反应完全,并有
也反应完全,并有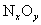 氮氧化物气体逸出.
氮氧化物气体逸出.
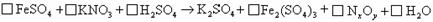
①推算出x=________,y=________. ②配平该化学方程式(系数填写在上式方框内)
③反应中氧化剂为________. ④用短线和箭头标出电子转移的方向和总数.
(2)油画所用颜料含有某种白色的铅化合物,置于空气中,天长日久就会生成黑色PbS,从而使油画的色彩变暗,若用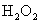 来“清洗”,则可将PbS转变为白色的
来“清洗”,则可将PbS转变为白色的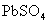 而使油画“复原”.请填空:①上述“清洗”反应的化学方程式为________________________________.
而使油画“复原”.请填空:①上述“清洗”反应的化学方程式为________________________________.
②若有0.1 mol的PbS参加反应,则在此反应中发生转移的电子为________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。 请回答:

查看答案和解析>>
科目:高中化学 来源: 题型:
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
由于浓度不同而能发生不同氧化还原反应的是 ( )
A.①③ B.③④ C.①② D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
锌和二氧化锰是电池工业中的主要原料,其中一种Zn—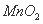 同槽电解的工业生产试验工艺流程涉及的主要反应有: ①
同槽电解的工业生产试验工艺流程涉及的主要反应有: ①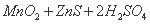 ===
===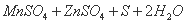
 ②
②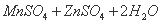
 下列说法正确的是( )
下列说法正确的是( )
A.①中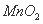 是氧化剂
是氧化剂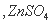 是还原产物
是还原产物
B.①中每产生16 g S时转移电子的物质的量为2 mol
C.按照②电解时,生成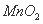 的电极为阴极
的电极为阴极
D.该工艺流程中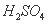 可循环
可循环
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧具有强氧化性,可使湿润的碘化钾淀粉试纸变蓝,有关反应如下:
O3+2KI+H2O===2KOH+I2+O2 ,下列对于此反应的说法正确的是( )
A.反应中,O3是氧化剂,H2O和KI是还原剂
B.氧化产物I2与还原产物O2的物质的量之比为1∶1
C.在反应中,1 mol O3得2 mol电子
D.由此反应可知,氧化性强弱顺序为:O3>I2>O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.其他条件不变,增大某一反应物的浓度,反应物的转化率一定都增大
B.对于有气体参加的反应,其他条件不变,增大压强,体积缩小,体系中各气体的浓度一定增大
C.对于有气体参加的反应,改变压强使平衡向右移动,生成的气体的浓度一定增大
D.增大反应物的浓度,平衡向右移动,生成物的体积分数一定增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com