
某稀溶液中含4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol铁,充分反应后产生的NO气体在标准状况下的体积为( )
A.36 L B.28 L
C.22.4 L D.11.2 L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
原子结构模型的演变图如右:
 |
其中,⑴为道尔顿实心球式原子模型、⑵为卢瑟福行星运转式原子模型、⑶为汤姆生葡萄干面包式原子模型、⑷为近代量子力学原子模型、⑸为玻尔轨道式原子模型。下列符合历史演变顺序的一组排列是( )
A.⑴⑵⑶⑷⑸ B.⑴⑶⑵⑸⑷ C.⑴⑸⑶⑵⑷ D.⑴⑶⑸⑷⑵
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在agHmX中所含质子的物质的量是( )
A.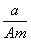 (A-N+m)mol B.
(A-N+m)mol B.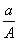 (A-N)mol
(A-N)mol
C.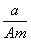 (A-N)mol D.
(A-N)mol D.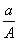 (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐
酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原
理制取少量Cl2。现将214.5gCa(ClO)2放入500 mL 12.0 mol/L的浓盐酸中,生成的Cl2
在标准状况下的体积为39.2 L。试计算:
(1)该反应消耗的氧化剂的质量是
(2)若反应前后溶液的体积保持不变,则反应后溶液中HCl的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将22.4 L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积变为11.2 L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A.NO2 B.N2O3
C.N2O D.N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
在某体系内有反应物和生成物5种物质:H2S、S、FeCl3、FeCl2、HCl.已知H2S为反应物,则另一反应物是( )
A.FeCl3 B.FeCl2 C.S D.HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
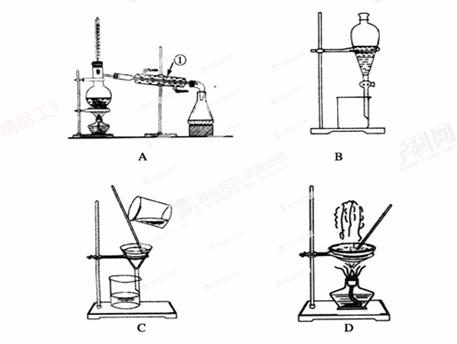
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中 的Cl-等杂质,选择装置________________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________________。
(3)装置A中①的名称是________,进水的方向是从________口进水。装置B在分液时为使液体顺利下滴,应进行的具体操作是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F六种常见物质,其转化关系如下图所示(部分反应条件和产物已略去)。已知A、B、C三种单质分别为固体、黄绿色气体、无色气体,D、E、F为化合物,D溶液呈黄色,E溶液显酸性。
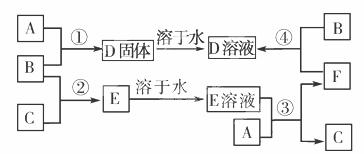
请回答下列问题:
(1)写出D的化学式 。
(2)写出D溶液与A反应的离子方程式 。
(3)写出反应④的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com