
一定条件下,化学反应2H2+O2===2H2O的能量变化如图所示,则反应的热化学方程式可表示为( )
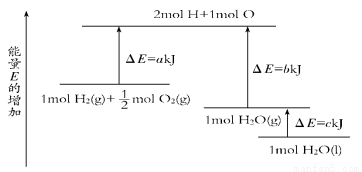
A.H2(g)+1/2O2(g)===H2O(g) ΔH=(a+b) kJ·mol-1
B.2H2(g)+O2(g)===2H2O(g) ΔH=2(b-a) kJ·mol-1
C.H2(g)+1/2O2(g)===H2O(l) ΔH=(b+c-a) kJ·mol-1
D.2H2(g)+O2(g)===2H2O(l) ΔH=2(a-b-c) kJ·mol-1
科目:高中化学 来源:2016届湖北省师大一附高三5月月考理综化学试卷(解析版) 题型:选择题
右下表为元素周期表的一部分。X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍。下列说法正确的是()

A.根据元素周期律,可以推测存在T3Y4、TZ2和TW4
B.X氢化物的沸点一定比Y氢化物的沸点高
C.XZ2、XW4与YW3都是非极性分子
D.W的氧化物的水化物酸性一定比Z的强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期中化学试卷(解析版) 题型:选择题
如图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
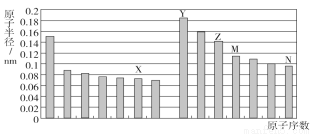
A.Z、N两种元素的离子半径相比,前者较大
B.X、N两种元素的气态氢化物的稳定性相比,前者较弱
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:填空题
元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下面是八种短周期元素的相关信息(已知铍的原子半径为0.089 nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色。
(1)C元素在元素周期表中的位置 。B形成的简单离子的结构示意图 。
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是 (填化学式)。
(3)用电子式表示A、D形成化合物的过程: 。
(4)H、E形成原子个数比为1∶1的化合物中所含化学键类型为 。
(5)GE2的电子式为 ,F与G形成的最简单的化合物的结构式为 。
(6)E的氢化物比C的氢化物的熔沸点高的原因是 。
(7)A、B、C、E原子半径由大到小的顺序为(用元素符号表示) 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
将4 mol A气体和2 mol B气体在2 L的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
A.反应过程中,当A、B、C的物质的量浓度之比为2∶1∶2时,反应即达到平衡状态
B.4 s内用物质B表示的反应速率为0.075 mol/(L·s)
C.达平衡后若增大压强,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是
A.反应混合物的浓度 B.反应体系的压强
C.正、逆反应的速率 D.反应物的转化率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下第一次月考化学试卷(解析版) 题型:填空题
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子的第一至第四电离能如下: |
I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中未成对电子最多的元素 |
G的3d能级只含有2对成对电子 |
(1)已知B2A4是一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,能很好地混溶于水,遇卤素、过氧化氢等强氧化剂作用能自燃。B2A4属于__________分子(填“极性”或“非极性”),B2A4分子中B原子轨道的杂化形式为___________。写出B2A4的电子式:___________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈____形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背了__________________。
该同学所画的电子排布图违背了__________________。
(4)分析DE3分子的空间构型为__________________。
(5)G位于________族________区,该元素的核外电子排布式为_________________。
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂。
GE2+xH2O=GE2·xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2·xH2O 119g。
①水合物中x=________。
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1∶1,则其化学式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下第一次月考化学试卷(解析版) 题型:选择题
右图三条曲线表示C、Si和P元素的四级电离能变化趋势。下列说法正确的是( )
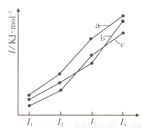
A.电负性:c>b>a B.最简单氢化物的稳定性:c>a>b
C.I5:a>c>b D.最简单氢化物的沸点:a>b>c
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 104 | 66 |
主要化合价 | +2 | +3 | +6、+4、-2 | -2 |
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW3
C.Y的氧化物对应的水化物一种是强酸
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com