
 ”°µĶĢ¼Ń»·”±”¢ČēŗĪ½µµĶ“óĘųÖŠCO2µÄŗ¬Į攢ӊŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŅżĘšĮĖČ«ŹĄ½ēµÄĘÕ±éÖŲŹÓ£®
”°µĶĢ¼Ń»·”±”¢ČēŗĪ½µµĶ“óĘųÖŠCO2µÄŗ¬Į攢ӊŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŅżĘšĮĖČ«ŹĄ½ēµÄĘÕ±éÖŲŹÓ£®| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ£Ømol£© | Ę½ŗāĮæ£Ømol£© | “ļµ½Ę½ŗāĖłŠčŅŖŹ±¼ä/min | ||
| CO£Øg£© | H2O£Øg£© | CO2£Øg£© | H2£Øg£© | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | tm |
| III | 900 | 2 | 4 | y | y | tn |
·ÖĪö I”¢øł¾ŻŃõ»Æ»¹Ō·“Ó¦Ńõ»Æ¼Į”¢»¹Ō¼ĮµĆŹ§µē×ÓŹżÄæĻąµČÅäĘ½£»
II”¢£Ø1£©øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖćv£ØH2£©£¬ŌŁĄūÓĆĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č¼ĘĖćv£ØCO2£©£»
£Ø2£©·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬Ķ¬ÖÖĪļÖŹµÄÕż”¢Äę·“Ó¦ĖŁĀŹĻąµČ£¬Ę½ŗāŹ±ø÷×é·ÖµÄĪļÖŹµÄĮ攢ÅØ¶Č”¢ŗ¬ĮæµČ²»ŌŁ·¢Éś±ä»Æ£¬ŅŌ¼°ÓÉ“ĖŃÜÉśµÄĘäĖüĮæ²»±ä£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£»
£Ø3£©IIŗĶIIIĪŖĶ¬ĪĀĻĀµÄ·“Ó¦£¬IIIĻąµ±ÓŚŌŚIIµÄ»ł“”ÉĻŌö“óĮĖ·“Ó¦ĪļµÄÅØ¶Č£¬Ōö“óŅ»±¶£¬¾Ż“Ė½ā“š¼“æÉ£»
£Ø4£©ÓÉĶ¼æÉÖŖ£¬bµćµÄ×Ŗ»ÆĀŹ²»ŹĒ×īøߣ¬¹ŹÕż·“Ó¦ĖŁĀŹøßÓŚÄę·“Ó¦ĖŁĀŹ£®
½ā“š ½ā£ŗI”¢·“Ó¦ÖŠCŌŖĖŲ»ÆŗĻ¼Ū0”ś+4£¬MnŌŖĖŲ»ÆŗĻ¼Ū+7”ś+2£¬·“Ó¦µĆŹ§µē×ÓĻąµČ£¬ŌņÓŠ£ŗ5C”«4KMnO4£¬ŌņÅäĘ½ŗóµÄ¼ĘĮæŹż·Ö±šŹĒ£ŗ5”¢4”¢5”¢4”¢2£¬¹Ź“š°øĪŖ£ŗ5”¢4”¢5”¢4”¢2£»
II£®£Ø1£©v£ØH2£©=$\frac{\frac{1mol}{2L}}{5min}$=0.1mol•£ØL•min£©-1£¬ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®£¬Ōņv£ØCO2£©=0.1mol•£ØL•min£©-1£¬¹Ź“š°øĪŖ£ŗ0.1£»
£Ø2£©A£®·“Ó¦Ē°ŗóĘųĢåµÄĪļÖŹµÄĮæ²»·¢Éś±ä»Æ£¬ČŻĘ÷ÖŠŹ¼ÖÕŃ¹Ēæ²»±ä£¬²»ÄÜĖµĆ÷·“Ó¦µ½“ļĘ½ŗā£¬¹ŹA“ķĪó£»
B£® ČŻĘ÷µÄĢå»żĪŖ2L£¬³õŹ¼ÅضČ=1mol/L
CO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©
æŖŹ¼£Ømol/L£©1 1 0 0
×Ŗ»Æ 0.5 0.5 0.5 0.5
Ę½ŗā 0.5 0.5 0.5 0.5
800ÉćŹĻ¶ČK=$\frac{0.5”Į0.5}{0.5”Į0.5}$=1£¬K=2²»ÄÜĖµĆ÷Ę½ŗā£¬¹ŹB“ķĪó£»
C£®ČŻĘ÷Ģå»ż²»±ä£¬ĘųĢåµÄÖŹĮæ²»±ä£¬¹ŹĆܶȏ¼ÖÕ²»±ä£¬¹ŹĆÜ¶Č²»±ä²»ÄÜĖµĆ÷“ļµ½Ę½ŗā£¬¹ŹC“ķĪó£»
D£®øł¾Ż·“Ó¦æÉÖŖ£¬¦ŌÕż£ØCO£©=¦ŌÄę£ØCO2£©ÄÜĖµĆ÷·“Ó¦µ½“ļĘ½ŗā£¬¹ŹDÕżČ·£¬¹ŹŃ”D£»
£Ø3£©IIŗĶIIIŌŚĶ¬Ņ»Ģõ¼žĻĀ½ųŠŠ£¬IIIÖŠĪļÖŹµÄĮæŹĒIIÖŠµÄ2±¶£¬“ļµ½Ę½ŗāKÖµ²»±ä£¬¹Źy=2”Į0.5=1£¬¹Ź“š°øĪŖ£ŗ1£»
£Ø4£©ÓÉĶ¼æÉÖŖ£¬bµćµÄ×Ŗ»ÆĀŹ²»ŹĒ×īøߣ¬¹ŹÕż·“Ó¦ĖŁĀŹøßÓŚÄę·“Ó¦ĖŁĀŹ£¬¼“¦ŌÕż£¾¦ŌÄę£»¹Ź“š°øĪŖ£ŗ£¾£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģŅņĖŲ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ»ł±¾øÅÄīµÄĄķ½āŗĶÓ¦ÓƵÄ漲飬עŅā°ŃĪÕÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ£¬°ŃĪÕĢāøųŠÅĻ¢£¬Ń§»į·ÖĪöĶ¼Ļó£¬ÄѶČÖŠµČ£®


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČōŌŚŗćĪĀŗćŃ¹ĻĀ£ŗµ±x=1Ź±£¬°“1.5molA”¢1molC×÷ĪŖĘšŹ¼ĪļÖŹ£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżČŌĪŖa | |
| B£® | ČōŌŚŗćĪĀŗćČŻĻĀ£ŗµ±x=2Ź±£¬½«3molC×÷ĪŖĘšŹ¼ĪļÖŹ£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżČŌĪŖa | |
| C£® | ČōŌŚŗćĪĀŗćŃ¹ĻĀ£ŗµ±x=3Ź±£¬°“1molA”¢1molB”¢1molC×÷ĪŖĘšŹ¼ĪļÖŹ£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżĪŖa | |
| D£® | ČōŌŚŗćĪĀŗćČŻĻĀ£ŗ°“0.6molA”¢0.3molB”¢1.4molC×÷ĪŖĘšŹ¼ĪļÖŹ£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżČŌĪŖa£¬ŌņxĪŖ2»ņ3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼µÄČ¼ÉÕČČ“óÓŚ110.5 kJ•mol-1 | |
| B£® | ÅØĮņĖįÓėĻ”NaOHČÜŅŗ·“Ӧɜ³É1 molĖ®£¬·Å³ö57.3 kJČČĮæ | |
| C£® | ĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ•mol-1 | |
| D£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øl£© µÄ·“Ó¦ČČĪŖ”÷H=+571.6 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® |  | B£® | HC”ŌC-CH2-CH3 | C£® | CH2=C£ØCH3£©2 | D£® | CH2=CHCH=CH2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

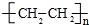 £¬øĆ·“Ó¦ŹōÓŚ¼Ó¾Ū·“Ó¦£»
£¬øĆ·“Ó¦ŹōÓŚ¼Ó¾Ū·“Ó¦£»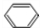 +Br2$\stackrel{FeBr_{3}}{”ś}$
+Br2$\stackrel{FeBr_{3}}{”ś}$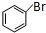 +HBr£®
+HBr£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4O | B£® | CH3CH2OH | C£® |  | D£® | 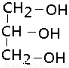 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņ¾ĆÖƵÄĀČĖ®ÖŠµĪČė×ĻÉ«ŹÆČļŹŌŅŗ£¬ČÜŅŗ½«ĻȱäŗģŗóĶŹÉ« | |
| B£® | Óū³żČ„Cl2ÖŠÉŁĮæHClĘųĢ壬æɽ«“Ė»ģŗĻĘųĢåĶعżŹ¢±„ŗĶŹ³ŃĪĖ®µÄĻ“ĘųĘæ | |
| C£® | ĘÆ°×·ŪµÄÓŠŠ§³É·ÖŹĒCaCl2ŗĶCa£ØClO£©2£¬Ó¦Ćܱձ£“ę | |
| D£® | ĀČĘųÓŠĘư׊Ō£¬ĖłŅŌĀČĘųÄÜŹ¹ÓŠÉ«²¼ĢõĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com