


 .
. .
. 、
、 、
、 任意2种.
任意2种. 分析 反应①是苯与丙烯发生加成反应生成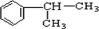 ,在光照条件下
,在光照条件下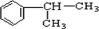 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为 ,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为
,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为 ,则C为
,则C为 ,结合根据产物可知D为
,结合根据产物可知D为 ,以此解答该题.
,以此解答该题.
解答 解:反应①是苯与丙烯发生加成反应生成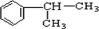 ,在光照条件下
,在光照条件下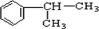 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为 ,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为
,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为 ,则C为
,则C为 ,结合根据产物可知D为
,结合根据产物可知D为 ,
,
( 1 )由上述分析可知,A 的结构简式可能为 ,故答案为:
,故答案为: ;
;
( 2)反应①是苯与丙烯发生加成反应生成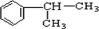 ,反应②是在光照条件下
,反应②是在光照条件下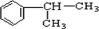 与氯气发生取代反应,反应③是A(卤代烃)在氢氧化钠醇溶液、加热条件下发生消去反应,故答案为:加成反应;取代反应;消去反应;
与氯气发生取代反应,反应③是A(卤代烃)在氢氧化钠醇溶液、加热条件下发生消去反应,故答案为:加成反应;取代反应;消去反应;
(3)反应④的化学方程式为: ,
,
故答案为: ;
;
(4)①该物质的水溶液遇FeCl3溶液呈紫色,说明含有酚羟基,
②分子中有苯环,且苯环上的一溴代物有两种,则苯环上有2个取代基,且位于对位位置,可能为 ,
,
故答案为: 、
、 、
、 任意2种.
任意2种.
点评 本题考查有机物的推断,题目难度中等,本题注意可用正逆推结合的方法推断,答题时注意把握题给信息,为解答该题的关键,注意同分异构体的判断.


科目:高中化学 来源: 题型:选择题
 已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )
已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )| A. | t2~t3 | B. | t0~t1 | C. | t4~t5 | D. | t6~t7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,反应MgCl2(1)═Mg(1)+Cl2(g)的△H>0,△S>0 | |
| B. | 水解反应NH+4+H2O?NH3•H2O+H+达到平衡后,升高温度平衡逆向移动 | |
| C. | 铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | |
| D. | 室温下向10mL pH=3的醋酸溶液中加水稀释后,溶液中导电粒子的数目减少. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂一般在过渡元素中寻找 | |
| B. | 过渡元素全部是金属元素,因此它们又被称为过渡金属 | |
| C. | 元素周期表中只有7个主族和7个副族 | |
| D. | 稀有气体元素原子的最外层电子数为2或者8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a的取值范围是$\frac{53}{84}$<a<$\frac{53}{62}$ | |
| B. | a=$\frac{53}{65}$,固体成分为碳酸钠和氢氧化钠 | |
| C. | a=$\frac{53}{75}$时,固体成分为碳酸钠 | |
| D. | 加热过程中产生二氧化碳的物质的量总是小于水的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BeCl2溶液的pH>7 | |
| B. | 蒸干Na2BeO2溶液并灼烧后得到的固体为BeO | |
| C. | Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 | |
| D. | 工业上可通过电解BeCl2水溶液制取Be |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com