
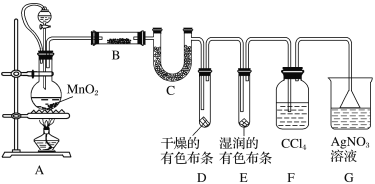
����Ŀ��ij��ѧʵ��С��Ϊ��̽����ʵ�����Ʊ�Cl2�Ĺ�������ˮ������HCl�ӷ�������ͬʱ֤��������ijЩ���ʣ�ijͬѧ�������ͼ��ʾ��ʵ��װ�ã�����������CCl4��HCl������CCl4)��
��ش��������⣺
��1��װ��A��������Ƥ�ܵ�Ŀ����___��
��2��װ��A�з�����Ӧ�����ӷ���ʽΪ___��װ��B��ʢ�ŵ��Լ���__��
��3����ͬѧ����ʵ����Ͻ��Կ��ǣ���Ϊ����F��G����װ��֮���ټ�һ��װ��ʪ��ĵ���KI��ֽ��װ�ã���Ŀ����___��
���𰸡�ʹ����ѹǿ�ȣ������ڷ�Һ©���е�Ũ����˳������ MnO2��4H����2Cl-=Mn2����Cl2����2H2O ��ˮ����ͭ ��֤HCl�е�Cl2�Ѿ���ȫ��ȥ������֤�Ƿ���Cl2��
��������
��1����Ƥ�ܿ��Խ���ƿ�ͷ�Һ©������������ƽ����ߵ�ѹǿ��ʹ��Һ��˳�����£�
��2��A��ʵ������ȡ������װ�ã��������Ҫ��Ҫ�����Ƿ���ˮ������![]() �ӷ�������G��װ����������Һ���Լ���ӷ�����
�ӷ�������G��װ����������Һ���Լ���ӷ�����![]() �����B�п���װ��ˮ����ͭ������ˮ������
�����B�п���װ��ˮ����ͭ������ˮ������
��3��������ˮ��ӦҲ��õ�![]() ��F��������������������ֹ��G�ļ���
��F��������������������ֹ��G�ļ���![]() ��ɸ��ţ�����Ӧ����F��G֮���һ��װ�������������Ƿ��ѳ�����
��ɸ��ţ�����Ӧ����F��G֮���һ��װ�������������Ƿ��ѳ�����
��1����Ƥ�ܵ�������ʹ����ѹǿ�ȣ������ڷ�Һ©���е�Ũ����˳�����£�
��2��װ��A�з�Ӧ�����ӷ���ʽΪ![]() ��B��ʢ�ŵ��Լ�����ˮ����ͭ��
��B��ʢ�ŵ��Լ�����ˮ����ͭ��
��3��Ŀ������֤![]() �е������Ƿ��ѳ�����
�е������Ƿ��ѳ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
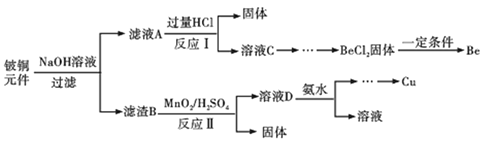
����Ŀ����ͭ����ѧ����ѧ�ۺ��������õĺϽ𣬹㷺Ӧ�������������Ԫ���������Ǵ�ij�Ͼ��ͭԪ������BeO25%��CuS71%������FeS��SiO2���л������ͭ���ֽ��������̡�
��֪��
���롢��Ԫ�ش������ڱ��еĶԽ���λ�ã���ѧ��������
�����£�Ksp[Cu��OH��2]=2.2��10-20��Ksp[Fe��OH��3]=4.0��10-38��Ksp[Mn��OH��2]=2.1��10-13
(1)����B����Ҫ�ɷ�Ϊ______���ѧʽ����
(2)д����Ӧ���к��뻯������������ᷴӦ�Ļ�ѧ����ʽ______��
(3)MnO2�ܽ����������е���Ԫ������Ϊ������д����Ӧ����CuS������Ӧ�����ӷ���ʽ______������ŨHNO3�ܽ��������ȱ����______����дһ������
(4)��BeCl2��Һ�еõ�BeCl2����IJ�����______��
(5)��ҺD�к�c��Cu2+��=2.2molL-1��c��Fe3+��=0.008molL-1��c��Mn2+��=0.01molL-1����μ���ϡ��ˮ����pH�����η������ȳ�������______�������ӷ��ţ���Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����______��
(6)ȡ��ͭԪ��1000g�����ջ��Be������Ϊ72g����Be�IJ�����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
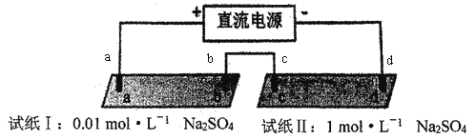
����Ŀ��̽���糡�������������ӵ�Ǩ�ơ�a��b��c��d ��Ϊʯī�缫���缫���4cm����pH��ֽ�ò�ͬŨ��Na2SO4��Һ�����ʪ����������ʵ�飬����˵������ȷ���ǣ� ��
ʵ������
ʱ�� | ��ֽI | ��ֽII |
lmin | a��������ֽ��죬b��������ֽ���� | c��������ֽ��죬d��������ֽ���� |
10min | ��ɫ������ɫ���������м���չ������ʱ��ɫ��Լ2.7cm����ɫ��Լ1.3cm | ������ɫ��Χ�������ԣ���ֽ����Ϊ��ɫ |
A. Na2SO4��Һ��SO42����a����c���ƶ�
B. a��������ֽ����ԭ���ǣ�2H2O+2e��= H2��+2OH��
C. ��ֽI������˵�����˻�����H+��Ǩ�����ʱ�OH����
D. �Ա���ֽI����ֽII������˵�������Ũ�Ⱥͻ���Ӱ��H+��OH����Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ 3 ��ʵ��װ�ã��ֱ�ش��������⡣
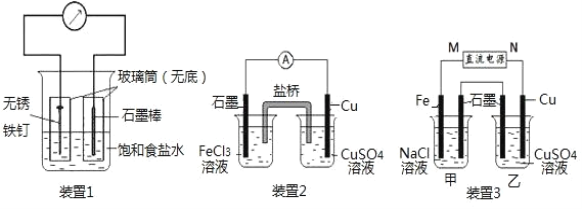
��1��װ�� 1 Ϊ����������ʴʵ�顣�����̼���IJ���Ͳ�ڵ����̪��Һ���ɹ۲쵽̼���������� Һ��죬�õ缫��ӦʽΪ_____��
��2��װ�� 2 �����Ϊ�Ȼ�����Һ���ҳ�Ϊ����ͭ��Һ��һ��ʱ����ҳ���Һ�� c��Cu2����_____(���������С�����䡱)������װ�õ�������ʢװ���� NH4NO3 ����֬��Һ���������е�_____���ӣ��NH4�� ����NO3���������Ȼ�����ҺǨ�ơ�
��3��װ�� 3 �м��ձ�ʢ�� 100mL 0.2mol/L �� NaCl ��Һ�����ձ�ʢ�� 100mL 0.5mol/L �� CuSO4 �� Һ����Ӧһ��ʱ��۲쵽���ձ���ʯī�缫�����������ɡ�
�ٵ�Դ�� M ��Ϊ��Դ_____����
�����ձ��е�ⷴӦ�����ӷ���ʽΪ_____��
��ֹͣ��⣬ȡ�� Cu �缫��ϴ�ӡ�����������缫���� 0.32g�����ձ��в����������״�������Ϊ_________mL��
����Ҫ���ҳ���Ƴɵ�⾫��ͭ��װ�ã����ҳص�ʯīӦ�ij�____�����ͭ����ͭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H����NH4����Mg2����Al3����Fe3����CO32����SO42����Cl���еļ��֡���������п����������ɫ��ζ�����壻��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ��������˵����ȷ����

A.��Һ�е�������ֻ��H����Mg2����Al3��
B.��Һ��һ������CO32����SO42�������ܺ���Cl��
C.��Һ��n(Mg2��)=0.1mol
D.n(H��) :n(NH4��) : n(Al3��) : n(Mg2��)=2:4:2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ΰ��Ͻ����ĸ���Һ�䷴Ӧ��Сʵ�飬���Ӧ��Ӧ�����ӷ���ʽ��д��ȷ����(����)
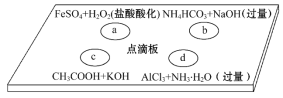
A. a��Ӧ��Fe2����2H����H2O2=Fe3����2H2O
B. b��Ӧ��HCO3-��OH��=CO32-��H2O
C. c��Ӧ��H����OH��=H2O
D. d��Ӧ��Al3����3NH3��H2O=Al(OH)3����3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2һ��-3���ȱ������ǰ�ɫ���壬���Ʊ��������£�

��֪��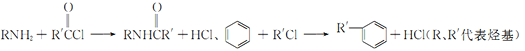
�ش������������
(1)![]() ��������__________��2������3���ȱ������к�N�����ŵĵ���ʽΪ__________��
��������__________��2������3���ȱ������к�N�����ŵĵ���ʽΪ__________��
(2)��Ӧ����R��������_____________����Ӧ�ڵķ�Ӧ����Ϊ_____________��
(3)�����Ӧ����KMnO4�Ļ�ԭ����ΪMnSO4����д���÷�Ӧ�Ļ�ѧ����ʽ_____________��
(4)A�Ľṹ��ʽΪ_____________���ķ�Ӧ����Ϊ_____________��
(5)��������������ͬ���칹��Ľṹ��ʽΪ_____________��
a.ʽ����![]() ��42�ı���ͬϵ�
��42�ı���ͬϵ�
b.������KMnO4��Ӧ�����ɶ�Ԫ����
c.����3�ֵ�Ч��
(6)��ʵ֤���������̵�Ŀ�����IJ��ʺܵͣ��ݴˣ��о���Ա�������������Ϊ������������������һ����ߡ�

����������ߵ�ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������Ͽ�ѧ�ҷ������������ᾧˮ�ľ�����5K�³��ֳ����ԡ��þ���Ļ�ѧʽΪNa0.35CoO2��1.3H2O(�þ����Ħ������Ϊ122g��mol-1)������NA��ʾ�����ӵ���������12.2g�þ����к���ԭ����Ϊ___����ԭ�ӵ����ʵ���Ϊ___mol��
��2��FeCl3��Һ����������ˮ����100mL2mol��L-1��FeCl3��Һ��ˮʱ�����ɾ��о�ˮ���õ�����___(����ڡ������ڡ���С�ڡ�)0.2NA��
��3���ڱ�״���£�VLij����(Ħ������ΪMg/mol)�ܽ���1Lˮ(ˮ���ܶȽ���Ϊ1g/cm3)�У�����������ȫ�ܽ��Ҳ���ˮ������Ӧ��������Һ���ܶ�Ϊ��g/cm3����������Һ�����ʵ���Ũ��c=___mol/L(��������ĸ��ʾ���ұ��뻯��)��
��4����ҵ�����������ƺ�ϡ����Ϊԭ���Ʊ�ClO2��Ӧ��NaClO2��HCl��ClO2����NaCl+H2O��д����ƽ�Ļ�ѧ����ʽ____��
��5����100mL��FeBr2��Һ��ͨ���״����Cl23.36L(��֪��ԭ�ԣ�Fe2����Br��)����Ӧ�����Һ��Cl����Br�������ʵ���Ũ����ȣ���ԭFeBr2��Һ�����ʵ���Ũ��Ϊ____mol/L����Ӧ�����ӷ���ʽΪ____��
��6������ʢ��10mL1mol��L��1NH4Al(SO4)2��Һ���ձ��м�20mL1.2mol��L��1Ba(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������������ȷ���ǣ� ��
A.78gNa2O2������ˮ��ַ�Ӧʱ����ת����ΪNA
B.2L1mol/LNa2SO4��Һ����������Ϊ3NA
C.25�棬101.3kPaʱ��11.2LH2�к��е�ԭ����ΪNA
D.4�棬101.3kPaʱ��54mlH2O�к��е�ԭ����Ϊ3NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com