
【题目】Ⅰ.⑴指出如下图实验装置中的错误之处(加热装置中烧杯底部已垫有石棉网)
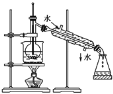
①____________________;
②____________________。
⑵图是某学生的过滤操作示意图,其操作不规范的是______

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
Ⅱ.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:


⑴指出提取碘的过程中有关实验操作①和②的名称:__________;________。
⑵在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的_____(注:试管中深色区为有色溶液),上层无色溶液的溶质是_____下层颜色是_____。
⑶从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是_______。
Ⅲ.某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:

欲证明滤液中存在SO42-、OH-,选用的方案是先取少量的滤液滴加________,发现溶液变红,再向其中加入________溶液,出现白色沉淀,则可证明SO42-、OH-,均存在。
【答案】冷凝水下进上出 温度计水银球伸入液面下 ade 过滤 萃取分液 D KCl 紫红色 蒸馏 酚酞 BaCl2
【解析】
Ⅰ.(1)蒸馏时温度计测定馏分的温度、冷却水下进上出;
(2)过滤时遵循一贴二低三靠,以此来解答。
Ⅱ.海藻灼烧得到海藻灰,浸泡得到悬浊液,过滤得到含I-离子的溶液通入氯气,氧化碘离子为碘单质,加入四氯化碳萃取剂分液,得到含碘单质的四氯化碳溶液,从有机溶液中提取碘,需要蒸馏操作。
Ⅲ.滴加酚酞变红可检验OH-,再加盐酸酸化,然后加氯化钡检验硫酸根离子;
Ⅰ.(1)图1实验装置中的错误之处为:温度计的水银球未在支管口处、冷却水未下进上出;
(2)a.漏斗末端颈尖未紧靠烧杯壁,会引起液体飞溅,故a错误;
b.玻璃棒用作引流可使液体流下,操作合理,故正确;
c.将滤纸湿润,使其紧贴漏斗壁,防止漏液,操作合理,故正确;
d.滤纸边缘应低于漏斗的边缘,故错误;
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度,可能将滤纸捅破,故错误。
故选 ade。
Ⅱ.(1)海藻灼烧得到海藻灰,浸泡得到悬浊液,过滤适用于不溶于水的固体和液体,分离固体和液体用过滤,过滤得到含I-离子的溶液通入氯气,氧化碘离子为碘单质,将碘水中的碘单质萃取出来,选择合适的萃取剂即可,加入四氯化碳萃取剂分液,得到含碘单质的四氯化碳溶液,从有机溶液中提取碘,①和②的名称:过滤;萃取分液。
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象,上层是水层,3mL,呈无色,下层1mL是有机层,呈紫红色,故选上图中的D,上层无色溶液的溶质是KCl,下层颜色是紫红色。
(3)从含碘的有机溶液中提取碘和回收有机溶剂,利用沸点不同,还需经过的操作是蒸馏。
Ⅲ.欲证明滤液中存在SO42-、OH-,选用的方案是先取少量的滤液滴加酚酞,发现溶液变红,再向其中加入盐酸、氯化钡溶液,出现白色沉淀,则可证明SO42-、OH- 均存在。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列七种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④CH3COONa ⑤CH3COOH ⑥NaHCO3
(1)溶液呈酸性的有_____________,呈碱性的有____________
(2)分别写出②、④水解的离子方程式:_____________________________、_____________________________。
(3)常温下,浓度均为0.1mol/L的③和⑥的溶液中离子种类_____________(填“相同”或“不相同”),溶液的PH:③_________⑥(填 >、=或 <)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.6 g H2O的物质的量是____,含有水分子的数目是_____,含有氢原子的物质的量是_____。
(2)1.5molCO2和______g CH4在标准状况下占有相同的体积,其体积为________。
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量为________。
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则:该气体的物质的量为______mol;一个X原子的质量为_______g;该气体在标准状况下的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数,则下列叙述不正确的是( )
A.所得溶液的体积为(36.5+1000)/ρ
B.所得溶液的物质的量浓度为![]()
C.所得溶液的溶解度为S=100w/(1-w)
D.所得溶液的质量分数:w=36.5c/1000ρ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢分解反应过程中,能量变化如图所示:下列说法正确的是

A. 催化剂可以改变过氧化氢分解反应的焓变
B. CuCl2或FeCl3可以催化H2O2分解反应
C. 催化剂不能改变反应路径
D. H2O2分解是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述中正确的是
A. 任何能使熵值增大的过程都能自发进行
B. △H<0,△S>0的化学反应一定能自发进行
C. 已知热化学方程式2SO2(g)+O2(g)![]() 2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量
D. 稀溶液中1mol NaOH分别和1mol CH3COOH、1molHNO3反应,两者放出的热量一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO+H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+ H2O(g)═CO(g)+3H2(g) ΔH。
已知:①CH4、H2、CO的燃烧热分别为a ![]() 、b
、b ![]() 、c
、c ![]() (a、b、c均大于0);
(a、b、c均大于0);
②水的汽化热为+d ![]() (d >0)。则ΔH=__________
(d >0)。则ΔH=__________![]() (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
(2)用合成气制甲醇的反应为2H2(g)+CO(g)![]() CH3OH(g) ΔH,在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示。
CH3OH(g) ΔH,在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示。

①ΔH________(填“>”“<”或“=”)0。
②写出两条可同时提高反应速率和CO的转化率的措施:_______、_____。
③下列说法正确的是___________(填序号)。
A.温度越高,该反应的平衡常数越大
B.达平衡后再充入稀有气体,CO的转化率提高
C.体系内气体压强不再变化时,反应达到平衡状态
D.图中压强p1<p2
④200 ℃时,n(H2)随时间的变化如表所示,3 min时反应刚好达到平衡状态,请利用表中的数据计算0~3 min内v(CH3OH)=_______![]() 。
。
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
⑤200℃时该反应的平衡常数K=____________。向上述200 ℃的平衡体系中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则平衡_______(填“正向移动”“逆向移动”或“不移动”)。
(3)甲、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷时,测得电路中转移1.96 mol电子,则甲烷的利用率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10 mL0.1mol/LHR溶液中逐滴滴入0.1mol/L的氨水,所得溶液pH 及导电能力与加入氨水体积的关系如图。下列说法不正确的是

A. 常温下,电离平衡常数 Ka(HR)≈Kb(NH3 H2O)
B. b点溶液pH=7,此时HR溶液与氨水恰好完全反应
C. c 点溶液中存在 c(NH4+ )>c(R- )>c(OH- )>c(H+)
D.a、b、c三点中,c点NH3 H2O的电离程度最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com