
| A£® | Ba£ØOH£©2•8H2OŗĶNH4Cl£Øs£©»ģŗĻ·“Ó¦ | B£® | ÉśŹÆ»ŅŗĶĖ®µÄ·“Ó¦ | ||
| C£® | ŅŗĢ¬Ė®Ęų»Æ | D£® | ŃĪĖįÓėĒāŃõ»ÆÄĘČÜŅŗµÄ·“Ó¦ |
·ÖĪö ³£¼ūµÄ·ÅČČ·“Ó¦ÓŠ£ŗĖłÓŠµÄĪļÖŹČ¼ÉÕ”¢ĖłÓŠ½šŹōÓėĖį»ņÓėĖ®”¢ĖłÓŠÖŠŗĶ·“Ó¦”¢¾ų“󶹏ż»ÆŗĻ·“Ó¦”¢ĀĮČČ·“Ó¦£»
³£¼ūµÄĪüČČ·“Ó¦ÓŠ£ŗ¾ų“óŹż·Ö½ā·“Ó¦”¢øö±šµÄ»ÆŗĻ·“Ó¦£ØČēCŗĶCO2£©”¢¹¤ŅµÖĘĖ®ĆŗĘų”¢Ģ¼£ØŅ»Ńõ»ÆĢ¼”¢ĒāĘų£©»¹Ō½šŹōŃõ»ÆĪļ”¢Ä³Š©ø“·Ö½ā£ØČēļ§ŃĪŗĶĒæ¼ī£©£®
½ā“š ½ā£ŗA£®Ba£ØOH£©2•8H2OŗĶNH4Cl£Ø¹ĢĢ壩·“Ó¦ŹĒĪüČČ·“Ó¦£¬ŌŚ·“Ó¦ÖŠĪüŹÕČČĮ棬¹ŹAÕżČ·£»
B£®ÉśŹÆ»ŅøśĖ®·“Ӧɜ³ÉŹģŹÆ»Ņ£¬·“Ó¦·Å³ö“óĮæµÄČČ£¬ŌņŹōÓŚ·ÅČČ·“Ó¦£¬¹ŹB“ķĪó£»
C£®ŅŗĢ¬Ė®Ęū»ÆĪüŹÕČČĮ棬µ«ŹōÓŚĪļĄķ±ä»Æ£¬²»ŹōÓŚĪüČČ·“Ó¦£¬¹ŹC“ķĪó£»
D£®ŃĪĖįÓėĒāŃõ»ÆÄĘČÜŅŗµÄ·“Ó¦£¬ŹōÓŚÖŠŗĶ·“Ó¦£¬ŹĒµäŠĶµÄ·ÅČČ·“Ó¦£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦µÄČČĮæ±ä»Æ£¬Ó¦×¢ÖŲ¹éÄÉ֊ѧ»Æѧ֊³£¼ūµÄĪüČČ»ņ·ÅČȵķ“Ó¦£¬¶ŌÓŚĢŲŹā¹ż³ĢÖŠµÄČČĮæ±ä»ÆµÄŅŖŹģĮ·¼ĒŅ䣬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
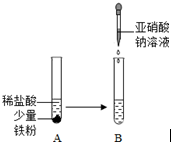
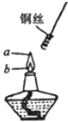 ČēĶ¼£¬Ä³Ķ¬Ń§×öŅŅ“¼Ńõ»ÆŹµŃ鏱£¬½«ĀŻŠż×“ĶĖæĻČ·Åµ½aµć“¦¼ÓČČ£¬Č»ŗóŌŁŅʵ½bµć£¬·¢ĻÖĶĖæŌŚ»šŃęa”¢bĮ½µćŹ±ĻÖĻóĆ÷ĻŌ²»Ķ¬£®ĒėÄ抓³öa”¢bĮ½µćµÄŹµŃéĻÖĻ󣬲¢½āŹĶ²śÉśøĆĻÖĻóµÄŌŅņ£¬²¢Š“³ö»Æѧ·“Ó¦·½³ĢŹ½£®
ČēĶ¼£¬Ä³Ķ¬Ń§×öŅŅ“¼Ńõ»ÆŹµŃ鏱£¬½«ĀŻŠż×“ĶĖæĻČ·Åµ½aµć“¦¼ÓČČ£¬Č»ŗóŌŁŅʵ½bµć£¬·¢ĻÖĶĖæŌŚ»šŃęa”¢bĮ½µćŹ±ĻÖĻóĆ÷ĻŌ²»Ķ¬£®ĒėÄ抓³öa”¢bĮ½µćµÄŹµŃéĻÖĻ󣬲¢½āŹĶ²śÉśøĆĻÖĻóµÄŌŅņ£¬²¢Š“³ö»Æѧ·“Ó¦·½³ĢŹ½£®| ŹµŃéĻÖĻó | ½āŹĶ | »Æѧ·½³ĢŹ½ | |
| a | |||
| b |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
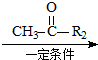 R1-CH=
R1-CH=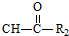 +H2O
+H2O 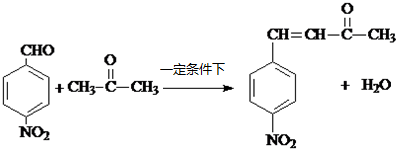
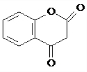 £®
£®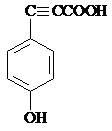 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
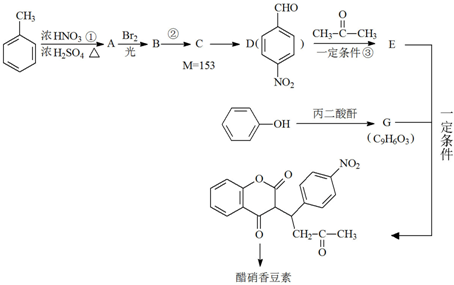
 ŃĒĻõĖįÄĘ£ØNaNO2£©Ė×³Ę¹¤ŅµŃĪ£¬Ķā¹ŪŗĶŹ³ŃĪĻąĖĘ£¬ÓŠĻĢĪ¶£¬Ņ×ČÜÓŚĖ®£¬Ė®ČÜŅŗĻŌ¼īŠŌ£¬¼ÓĒæČČŹ±ÄÜ·Ö½ā²śÉśÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ČĖČōĪóŹ³»įŅżĘšÖŠ¶¾£¬ÖĀĖĄĮæĪŖ0.3g”«0.5g£¬ĖüŹ¹ČĖÖŠ¶¾ŹĒŅņĪŖĖüÄܽ«ČĖĢåŃŖŗģµ°°×ÖŠµÄFe2+×Ŗ»ÆĪŖFe3+£¬“Ó¶ųŹ¹ŃŖŗģµ°°×É„Ź§ŠÆŃõÄÜĮ¦£®
ŃĒĻõĖįÄĘ£ØNaNO2£©Ė×³Ę¹¤ŅµŃĪ£¬Ķā¹ŪŗĶŹ³ŃĪĻąĖĘ£¬ÓŠĻĢĪ¶£¬Ņ×ČÜÓŚĖ®£¬Ė®ČÜŅŗĻŌ¼īŠŌ£¬¼ÓĒæČČŹ±ÄÜ·Ö½ā²śÉśÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ČĖČōĪóŹ³»įŅżĘšÖŠ¶¾£¬ÖĀĖĄĮæĪŖ0.3g”«0.5g£¬ĖüŹ¹ČĖÖŠ¶¾ŹĒŅņĪŖĖüÄܽ«ČĖĢåŃŖŗģµ°°×ÖŠµÄFe2+×Ŗ»ÆĪŖFe3+£¬“Ó¶ųŹ¹ŃŖŗģµ°°×É„Ź§ŠÆŃõÄÜĮ¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 10”ꏱ£¬20mL3mol/LµÄXČÜŅŗ | B£® | 20”ꏱ£¬30mL2mol/LµÄXČÜŅŗ | ||
| C£® | 20”ꏱ£¬20mL4mol/LµÄXČÜŅŗ | D£® | 10”ꏱ£¬10mL2mol/LµÄXČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2×÷ŗōĪüĆę¾ßÖŠµÄ¹©Ńõ¼Į | |
| B£® | Įņ»ĒÓĆÓŚÖĘ»šŅ© | |
| C£® | Ć¾ŗĻ½šÓĆÓŚÖĘŌģĘū³µ”¢·É»ś”¢»š¼ż | |
| D£® | BaCO3×÷”°±µ²Ķ”±--¼ģ²é³¦ĪøµÄÄŚ·žŅ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØĮņĖįÓėŗ¬ÓŠĖ®·ÖµÄÕįĢĒ×÷ÓĆĻŌŹ¾µÄŠŌÖŹŹĒĖįŠŌ”¢ĶŃĖ®ŠŌ”¢ĒæŃõ»ÆŠŌ”¢ĪüĖ®ŠŌ | |
| B£® | ¶žŃõ»Æ¹č²»ÓėČĪŗĪĖį·“Ó¦£¬æÉÓĆŹÆÓ¢ÖĘŌģÄĶĖįČŻĘ÷ | |
| C£® | ½«SO2ĶØČėĘ·ŗģČÜŅŗ£¬ČÜŅŗĶŹÉ«ŗó¼ÓČČ»Öø“ŌÉ«£»½«SO2ĶØČėäåĖ®£¬äåĖ®ĶŹÉ«ŗó¼ÓČČ²»ÄÜ»Öø“ŌÉ« | |
| D£® | ĶµÄ½šŹō»īĘĆŠŌ±ČĢśµÄ²ī£¬æÉŌŚŗ£ĀÖĶāæĒÉĻ×°ČōøÉĶæéŅŌ¼õ»ŗĢśøÆŹ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com