
 ¹¤ŅµÉĻæÉŅŌŅŌĆŗŗĶĖ®ĪŖŌĮĻĶعżŅ»ĻµĮŠ×Ŗ»Æ±äĪŖĒå½ąÄÜŌ“ĒāĘų»ņ¹¤ŅµŌĮĻ¼×“¼£®
¹¤ŅµÉĻæÉŅŌŅŌĆŗŗĶĖ®ĪŖŌĮĻĶعżŅ»ĻµĮŠ×Ŗ»Æ±äĪŖĒå½ąÄÜŌ“ĒāĘų»ņ¹¤ŅµŌĮĻ¼×“¼£®·ÖĪö £Ø1£©·“Ó¦ČČÓėĪļÖŹµÄ¾Ū¼ÆדĢ¬ÓŠ¹Ų£¬¾Ū¼ÆדĢ¬²»Ķ¬£¬·“Ó¦ČČ²»Ķ¬£»
£Ø2£©¢ŁæÉÄę·“Ó¦ÖŠŌö“óŅ»ÖÖ·“Ó¦ĪļÅضČæÉŅŌĢįøßĮķŅ»ÖÖ·“Ó¦Īļ×Ŗ»ÆĀŹ£»
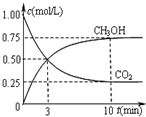
ŅĄ¾ŻCO2£Øg£©+3H2£Øg£©ØTCH3OH£Øg£©+H2O£Øg£©”÷H£¼0ĪŖĘųĢåĢå»ż¼õŠ”µÄ”¢·ÅČČ·“Ó¦ĢŲµć½įŗĻÓ°Ļģ»ÆŃ§Ę½ŗāŅĘ¶ÆµÄŅņĖŲ½ā“š£»
¢Ś£®¢”£®¼ĘĖćĘ½ŗāŹ±ĒāĘų”¢Ė®µÄÅØ¶Č£¬ŌŁøł¾ŻK=$\frac{c£ØCH{\;}_{3}OH£©”Įc£Ø{H}_{2}O£©}{c£ØCO{\;}_{2}£©”Į{c}^{3}£ØH{\;}_{2}£©}$¼ĘĖćĘ½ŗā³£Źż£»
±£³ÖĪĀ¶Č²»±ä£¬ĻņøĆĆܱÕČŻĘ÷ÖŠŌŁ³äČė1mol CO2£Øg£©ŗĶ1mol H2O£Øg£©£¬Ļąµ±ÓŚŌö“óŃ¹Ē棬ŌöŃ¹Ę½ŗāĻņĘųĢåĻµŹżŠ”µÄ·½ĻņŅĘ¶Æ£»
¢¢£®Ę½ŗāŹ±Āś×ćVÕż=VÄę£¬vÕż=kÕż•c£ØA£©a•c£ØB£©b£»VÄę=kÄę•c£ØC£©c•c£ØD£©d£¬ŌņkÄę£ŗkÕż=$\frac{c£ØCH{\;}_{3}OH£©”Įc£Ø{H}_{2}O£©}{c£ØCO{\;}_{2}£©”Į{c}^{3}£ØH{\;}_{2}£©}$=K£»
¼ĘĖć3mimŹ±ø÷ĪļÖŹÅØ¶Č£¬¾Ż“Ė¼ĘĖćÕżÄę·“Ó¦Ė²Ź±ĖŁĀŹÖ®±Č£®
½ā“š ½ā£ŗ£Ø1£©·“Ó¦ČČÓėĪļÖŹµÄ¾Ū¼ÆדĢ¬ÓŠ¹Ų£¬¾Ū¼ÆדĢ¬²»Ķ¬£¬·“Ó¦ČČ²»Ķ¬£¬ÉĻŹö·“Ó¦ÓėĒāĘųČ¼ÉÕČȵķ“Ó¦ÖŠĖ®µÄדĢ¬²»Ķ¬£¬ĖłŅŌ²»ÄÜĒó³öÉĻŹö·“Ó¦µÄģŹ±ä£»
¹Ź“š°øĪŖ£ŗ²»ÄÜ£»ŅņĪŖÉĻŹö·“Ó¦ÓėĒāĘųČ¼ÉÕČȵķ“Ó¦ÖŠĖ®µÄדĢ¬²»Ķ¬£»
£Ø2£©¢ŁC£Øs£©+2H2O£Øg£©?CO2£Øg£©+2H2£Øg£©”÷H£¾0Éś³É¶žŃõ»ÆĢ¼ŗĶĒāĘųµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2£¬¶ų
CO2£Øg£©+3H2£Øg£©ØTCH3OH£Øg£©+H2O£Øg£©”÷H£¼0£¬¶žŃõ»ÆĢ¼ŗĶĒāĘųĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ3£¬Ļą¶ŌÓėŌö“ó¶žŃõ»ÆĢ¼ÅØ¶Č£¬ĖłŅŌĒāĘųµÄ×Ŗ»ÆĀŹ“óÓŚ¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ£»
CO2£Øg£©+3H2£Øg£©ØTCH3OH£Øg£©+H2O£Øg£©”÷H£¼0ĪŖĘųĢåĢå»ż¼õŠ”µÄ”¢·ÅČČ·“Ó¦£¬ŅŖĻėĢįø߼ד¼µÄ²śĀŹæÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ½µµĶĪĀ¶Č”¢Ōö“óŃ¹ĒæŹ¹Ę½ŗāĻņÕżĻņŅĘ¶Æ£»
¹Ź“š°øĪŖ£ŗŗóÕß“ó£»½µµĶĪĀ¶Č”¢Ōö“óŃ¹Ē棻
¢Ś¢”Ę½ŗāŹ±¼×“¼ĪŖ0.75mol/L”¢¶žŃõ»ÆĢ¼ĪŖ0.25mol/L£¬Ōņ£ŗ
CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©
ĘšŹ¼ÅØ¶Č£Ømol/L£©£ŗ1 3 0 0
±ä»ÆÅØ¶Č£Ømol/L£©£ŗ0.75 2.25 0.75 0.75
Ę½ŗāÅØ¶Č£Ømol/L£©£ŗ0.50 0.75 0.75 0.75
ŌņĘ½ŗā³£ŹżK=$\frac{c£ØCH{\;}_{3}OH£©”Įc£Ø{H}_{2}O£©}{c£ØCO{\;}_{2}£©”Į{c}^{3}£ØH{\;}_{2}£©}$=$\frac{0.75”Į0.75}{0.25”Į0.75{\;}^{3}}$=$\frac{16}{3}$=5.33£»
±£³ÖĪĀ¶Č²»±ä£¬ĻņøĆĆܱÕČŻĘ÷ÖŠŌŁ³äČė1mol CO2£Øg£©ŗĶ1mol H2O£Øg£©£¬Ļąµ±ÓŚŌö“óŃ¹Ē棬ŌöŃ¹Ę½ŗāĻņĘųĢåĻµŹżŠ”µÄ·½ĻņŅĘ¶Æ£¬¼“ĻņÕż·½ĻņŅĘ¶Æ£»
¹Ź“š°øĪŖ£ŗ5.33£»ÕżĻņ£»
¢¢Ę½ŗāŹ±Āś×ćVÕż=VÄę£¬vÕż=kÕż•c£ØA£©a•c£ØB£©b£»VÄę=kÄę•c£ØC£©c•c£ØD£©d£¬
ŌņkÄę£ŗkÕż=$\frac{c£ØCH{\;}_{3}OH£©”Įc£Ø{H}_{2}O£©}{c£ØCO{\;}_{2}£©”Į{c}^{3}£ØH{\;}_{2}£©}$=K=3£ŗ16£»
CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©
ĘšŹ¼ÅØ¶Č£Ømol/L£©£ŗ1 3 0 0
±ä»ÆÅØ¶Č£Ømol/L£©£ŗ0.50 1.50 0.50 0.50
3minÅØ¶Č£Ømol/L£©£ŗ0.50 1.50 0.50 0.50
vÕż=kÕż•c£ØA£©a•c£ØB£©b£»
VÄę=kÄę•c£ØC£©c•c£ØD£©d£»
VÕż£ŗVÄę=$\frac{{\;}_{kÕż}•c£ØA£©{\;}^{a}•c£ØB£©{\;}^{b}}{k{\;}_{Äę}•c£ØC£©{\;}^{c}•c£ØD£©{\;}^{d}}$=$\frac{{K}_{Õż}}{{K}_{Äę}}$•$\frac{0.5”Į1.5{\;}^{3}}{0.5”Į0.5}$=36£»
¹Ź“š°øĪŖ£ŗ3£ŗ16£» 36£®
µćĘĄ ±¾ĢāĪŖ×ŪŗĻĢā£¬Éę¼°·“Ó¦ČČµÄ¼ĘĖć”¢»ÆŃ§Ę½ŗāĘ½ŗāŅʶÆÓ°ĻģŅņĖŲ”¢»ÆŃ§Ę½ŗā³£Źż¼ĘĖć£¬ĢāÄæÄŃ¶Č½Ļ“󣬽āĢā¹Ų¼üŠčÕĘĪÕ»ÆŃ§Ę½ŗāĄķĀŪ£¬×¢ŅāČż¶ĪŹ½µÄÓ¦ÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molČŪČŚµÄKHSO4ÖŠŗ¬ÓŠ2 NAøöŃōĄė×Ó | |
| B£® | 1 L 0.1 mol/LCH3COONaČÜŅŗÖŠ£¬ŅõĄė×Ó×ÜŹżŠ”ÓŚ0.1 NA | |
| C£® | ±ź×¼×“æöĻĀ£¬6.72 L NO2ÓėĖ®³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA | |
| D£® | Óė³£ĪĀ³£Ń¹ĻĀ17g H2O2Ėłŗ¬·Ē¼«ŠŌ¼üŹżÄæĻąĶ¬µÄN2H4µÄ·Ö×Ó×ÜŹżĪŖ0.5NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XĒā»ÆĪļČÜÓŚĖ®ŗó£¬ŌŚ³£ĪĀĻĀ£¬øĆČÜŅŗµÄpH£¼7 | |
| B£® | YµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¾ßÓŠĮ½ŠŌ | |
| C£® | ZĄė×ÓŌŚĖ®ČÜŅŗÖŠĖ®½āµ¼ÖĀĘäČÜŅŗĻŌ¼īŠŌ | |
| D£® | ¼ņµ„Ąė×ӵİė¾¶£ŗY£¾Z£¾X |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéÓėŅŅĶéĢå»ż±ČĪŖ1£ŗ4 | B£® | ŅŅĻ©Óė¶”ĶéĢå»ż±ČĪŖ4£ŗ1 | ||
| C£® | ±ūČ²ÓėŅŅČ²ĪļÖŹµÄĮæ±ČĪŖ4£ŗ1 | D£® | ŅŅĻ©Óė¶”Ļ©ĪļÖŹµÄĮæ±ČĪŖ1£ŗ4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äåŅŅĶé | B£® | ĢģČ»Ęų | C£® | ŹÆÓĶ | D£® | ¾Ę¾« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ×éŗÅ | ·“Ó¦ĪĀ¶Č£Ø”ę£© | ²Ī¼Ó·“Ó¦µÄĪļÖŹ | ||||
| Na2S2O3 | H2SO4 | H2OµÄĢå»ż£ØmL£© | ||||
| Ģå»ż£ØmL£© | ÅØ¶Č£Ømol•L-1£© | Ģå»ż£ØmL£© | ÅØ¶Č£Ømol•L-1£© | |||
| A | 10 | 5.0 | 0.10 | 10.0 | 0.10 | 5.0 |
| B | 10 | 5.0 | 0.10 | 5.0 | 0.10 | 10.0 |
| C | 30 | 5.0 | 0.10 | 5.0 | 0.10 | 10.0 |
| D | 30 | 5.0 | 0.20 | 5.0 | 0.10 | 10.0 |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | a=b=100 | B£® | a=b=1000 | C£® | a£¼b | D£® | a£¾b |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com