
【题目】化合物Y具有保肝、抗炎、增强免疫等功效,可由X制得。下列有关化合物X、Y的说法正确的是

A.一定条件下X可发生氧化、取代、消去反应
B.1 mol Y最多能与4mol NaOH反应
C.X与足量H2反应后,每个产物分子中含有8个手性碳原子
D.等物质的量的X、Y分别与足量Br2反应,最多消耗Br2的物质的量相等
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】已知![]() 将硫酸铵完全分解后的气体通入过量
将硫酸铵完全分解后的气体通入过量![]() 溶液中,有白色沉淀生成且有无色无味气体逸出。说法正确的是
溶液中,有白色沉淀生成且有无色无味气体逸出。说法正确的是![]()
A.生成沉淀中有![]() 和
和![]() ,且
,且![]() :
:![]() 约为1:1
约为1:1
B.生成沉淀中有![]() 和
和![]() ,且
,且![]() :
:![]() 约为1:2
约为1:2
C.生成沉淀中有![]() 和
和![]() ,且
,且![]() :
:![]() 约为1:3
约为1:3
D.从溶液中逸出的气体只有![]() ,溶液中溶质只有
,溶液中溶质只有![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下元素同期表,以下说法正确的是

A. 白格中都是主族元素,灰格中都是副族元素
B. X、Y、Z元素分别为N、P、O
C. 原子半径:Z>X>Y
D. X、Y、Z的气态氢化物中稳定性最高的是X的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是( )
A.糖类、油脂、蛋白质都是有机高分子化合物
B.有机物![]() 可以发生消去反应和催化氧化
可以发生消去反应和催化氧化
C.乙醇可以和金属钠反应很缓慢地放出氢气,说明乙醇的酸性很弱
D.福尔马林可用作食品防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验现象得出的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 废FeCl3蚀刻液中加入少量铁粉,振荡 | 得到澄清溶液 | 蚀刻液中一定不含Cu2+ |
B | 将Fe(NO3)2样品溶于H2SO4,滴加KSCN溶液 | 溶液变红 | 稀硫酸能氧化Fe2+ |
C | 向两份蛋白质溶液中分别滴加饱和硫酸钠溶液和硫酸铜溶液 | 均有固体析出 | 蛋白质均发生变性 |
D | 葡萄糖溶液与新制Cu(OH)2混合加热 | 生成砖红色沉淀 | 葡萄糖分子中含有醛基 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒温、恒容的密闭容器中进行下列两个可逆反应:(甲)2X(g) ![]() Y(g)+Z(s) (乙)A(s)+2B(g)
Y(g)+Z(s) (乙)A(s)+2B(g) ![]() C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度;②反应容器中生成物的百分含量;③反应物的消耗速率与生成物的消耗速率之比等于系数之比;④混合气体的压强⑤混合气体的总物质的量。其中能表明(甲)和(乙)都达到化学平衡状态是( )
C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度;②反应容器中生成物的百分含量;③反应物的消耗速率与生成物的消耗速率之比等于系数之比;④混合气体的压强⑤混合气体的总物质的量。其中能表明(甲)和(乙)都达到化学平衡状态是( )
A.①②③B.①②③⑤C.①②③④D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,则 N4(g) = 2N2(g)ΔH为( )
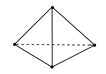
A.+882 kJ·mol-1B.-882kJ·mol-1C.+1216 kJ·mol-1D.-1216 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
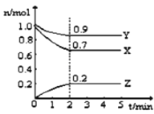
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2 、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
0~50s内的平均反应速率 v(N2) = __________,250s时,H2的转化率为____________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。![]() 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中___(填“吸收”或“放出”)的能量为____, 反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中___(填“吸收”或“放出”)的能量为____, 反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时____(填增大、减小或不变),混合气体密度比起始时______(填增大、减小或不变)。
(5)为加快反应速率,可以采取的措施是_______
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用电解锰阳极泥(主要成分MnO2、MnO)制备MnO2的工艺流程如下:
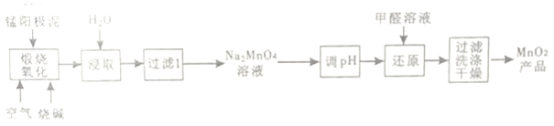
(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为___________;MnO2煅烧反应的化学方程式为__________________。
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有____________、____________(列举2点)
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和___________;写出用pH试纸测定溶液pH的操作_______________。
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为_____________。
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是_____________;产品中MnO2的质量分数为ω(MnO2)=____________(列出计算的表达式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com