
| n |
| V |
| 1mol |
| 0.1L |
| ||


科目:高中化学 来源: 题型:
| A、加入合金的质量可能为9.6g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH溶液体积为150mL |
| D、溶解合金时产生NO气体体积2.24L(STP) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
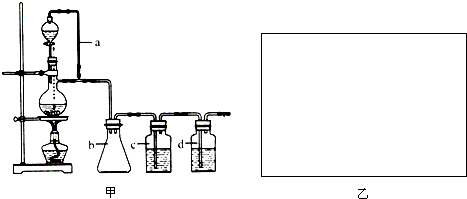
| 浓H2SO4 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铜钥匙做阳极,碳棒做阴极,CuSO4溶液做电解质溶液 |
| B、Zn与铜钥匙用导线相连插入ZnSO4溶液中 |
| C、Zn做阳极,铜钥匙做阴极,ZnSO4溶液做电镀液电解 |
| D、在电镀过程中溶液中的Zn2+浓度减小,Cu2+浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
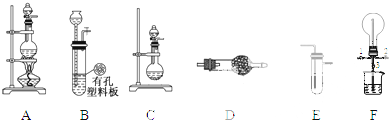
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、.①③④⑤ |
| C、①②③④⑤ | D、①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com