
 ��
�� ��
�� ��
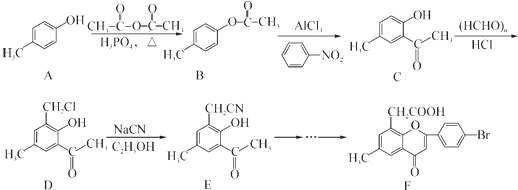
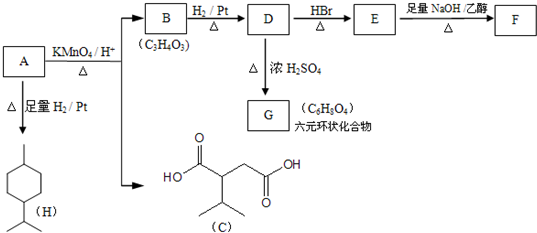
��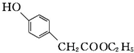 ����һ����Ҫ��ҽҩ�м��壮д����A���Ҵ�Ϊ��Ҫԭ���Ʊ����ǻ������������ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�
����һ����Ҫ��ҽҩ�м��壮д����A���Ҵ�Ϊ��Ҫԭ���Ʊ����ǻ������������ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�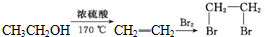
���� ��1����A��B�ṹ��ʽ��֪��AӦΪ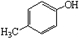 ������������Ӧ����B��
������������Ӧ����B��
��2������F�Ľṹ��ʽ��֪��F�к������������ƣ�
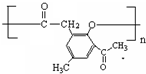
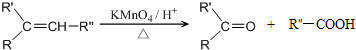
��3��Eˮ����ﺬ���Ȼ����ǻ�����ͨ�������������۷�Ӧ���ݴ��жϸ߷��ӻ�����Ľṹ��ʽ��
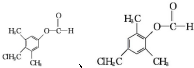
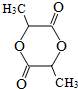
��4��D������ͬ���칹���������4�ֲ�ͬ��ѧ�������⣬�ɷ���ˮ�ⷴӦ����һ��ˮ���������FeCl3������ɫ��Ӧ����һ��ˮ������ܷ���������Ӧ����ӦΪ��������ǻ��γɵ������ݴ���дͬ���칹�壻
��5�� �ڹ��������·�Ӧ��������NaCN���Ҵ������·�Ӧ��ˮ�����������Ӧ�����ɲ��
�ڹ��������·�Ӧ��������NaCN���Ҵ������·�Ӧ��ˮ�����������Ӧ�����ɲ��
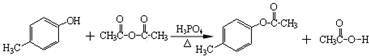
��� �⣺��1����A��B�ṹ��ʽ��֪��AӦΪ ������������Ӧ����B����Ӧ�ķ���ʽΪ
������������Ӧ����B����Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��2���ɽṹ��ʽ��֪F��������3�����������ţ����Ʒֱ�Ϊ�Ѽ����ʻ����Ȼ���
�ʴ�Ϊ���Ѽ����Ȼ���
��3��E����-CN��ˮ����ﺬ���Ȼ����ǻ����ɷ���������Ӧ��������Ϊ ��
��
�ʴ�Ϊ�� ��
��
��4��D������ͬ���칹���������4�ֲ�ͬ��ѧ�������⣬�ɷ���ˮ�ⷴӦ����һ��ˮ���������FeCl3������ɫ��Ӧ����һ��ˮ������ܷ���������Ӧ����ӦΪ��������ǻ��γɵ�������Ӧ�Ľṹ��ʽ��Ϊ ��
��
�ʴ�Ϊ�� ��
��
��5�� �ڹ��������·�Ӧ��������NaCN���Ҵ������·�Ӧ��ˮ�����������Ӧ�����ɲ������Ϊ
�ڹ��������·�Ӧ��������NaCN���Ҵ������·�Ӧ��ˮ�����������Ӧ�����ɲ������Ϊ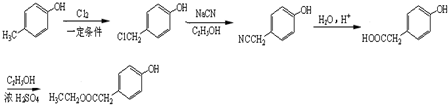 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ���Ŀ�ۺϿ���ѧ�����������������ۺ����û�ѧ֪ʶ��������Ϊ�߿��������ͣ�����ʱע����������Ϣ��Ϊ������Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
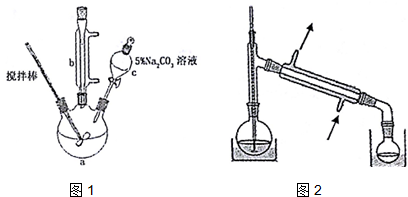
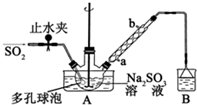 ���������Ƽ�ȩ��NaHSO2•HCHO•2H2O���׳Ƶ��飬���ȶ���120��ʱ��ֽ⣬��ӡȾ��ҽҩ�Լ�ԭ���ܹ�ҵ���й㷺Ӧ�ã���Na2SO3��SO2��HCHO��п��Ϊԭ���Ʊ����������Ƽ�ȩ��ʵ�鲽����ͼ��
���������Ƽ�ȩ��NaHSO2•HCHO•2H2O���׳Ƶ��飬���ȶ���120��ʱ��ֽ⣬��ӡȾ��ҽҩ�Լ�ԭ���ܹ�ҵ���й㷺Ӧ�ã���Na2SO3��SO2��HCHO��п��Ϊԭ���Ʊ����������Ƽ�ȩ��ʵ�鲽����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �ڢܢ� | C�� | �ڢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol KClO3 �μӷ�Ӧ��2mol����ת�� | |
| B�� | ClO2���������� | |
| C�� | H2C2O4��������ǿ��ClO2�������� | |
| D�� | KClO3 �ڷ�Ӧ�еõ����ӣ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �е� | �ܽ��� | ||
| ��ϩ�� | 141�� | ��ˮ���ܣ��������л��ܼ� | �ж� |
| �״� | 65�� | ��ˮ���ܣ��������л��ܼ� | �ӷ����ж� |
| ��ϩ����� | 80.5�� | ������ˮ���������л��ܼ� | �ӷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
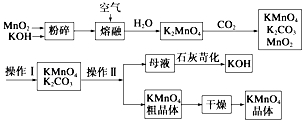 ������ؿ�������������������ѧ��ѧ����������������ҵ�ϣ������̿��Ƹ�����ص��������£�
������ؿ�������������������ѧ��ѧ����������������ҵ�ϣ������̿��Ƹ�����ص��������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �������� | ���� | ���� | ���� | ���� |
| �е㣨�棩 | -88.6 | -42.1 | -0.5 | 36.1 |
| *ȼ���ȣ�kJ•mol-1�� | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
| A�� | �������ڳ��³�ѹ�¿϶��������� | |
| B�� | ֱ������ȼ���Ⱥ�������̼ԭ���������Թ�ϵ | |
| C�� | ��̼ԭ�������ӣ�ֱ�������е������� | |
| D�� | ��̼ԭ�������ӣ�ֱ�������е��ȼ���ȶ��ɱ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
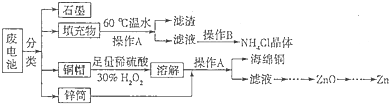
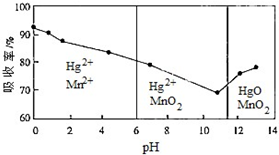
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com