
| A. | SO2与Si02 | B. | CCl4与KCl | C. | NaCl与HCl | D. | HNO3与H20 |
分析 根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键.
解答 解:A、固体SO2是分子晶体,二氧化硅是原子晶体,二氧化硅、二氧化碳都只含共价键,故A错误;
B、固体CCl4是分子晶体,只含有共价键,KCl是离子晶体,只含有离子键,故B错误;
C、NaCl是离子晶体,NaCl中只含离子键,固体HCl是分子晶体,HCl中只含共价键,故C错误;
D、HNO3和H20都是分子晶体,晶体中均含共价键,故D正确;
故选:D.
点评 本题考查了化学键类型和晶体类型的关系,判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键.


科目:高中化学 来源: 题型:解答题
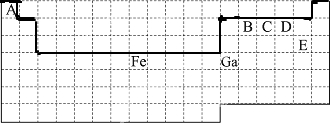 .
.
 、
、 (写2种).
(写2种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
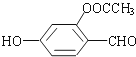 已知醛基能发生如下反应:2-CHO+OH-→CH2OH+COO-.则1mol如图所示的有机物与足量的NaOH溶液作用后,最多消耗NaOH的物质的量为( )
已知醛基能发生如下反应:2-CHO+OH-→CH2OH+COO-.则1mol如图所示的有机物与足量的NaOH溶液作用后,最多消耗NaOH的物质的量为( )| A. | 2.5mol | B. | 3mol | C. | 3.5 mol | D. | 4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时 NH4Cl 溶液的 KW 大于 100℃时 NaCl 溶液的 KW | |
| B. | SO2 通入碘水中,反应的离子方程式为 SO2+I2+2H2O═SO32-+2I-+4H+ | |
| C. | 加入铝粉能产生 H2 的溶液中,可能存在大量的 Na+、Ba2+、AlO2-、NO3- | |
| D. | 100℃时,将 pH=2 的盐酸与 pH=12 的 NaOH 溶液等体积混合,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
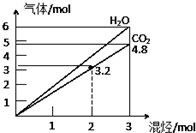 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )| A. | ①②④ | B. | ②④⑤ | C. | ②③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
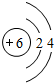
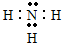
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
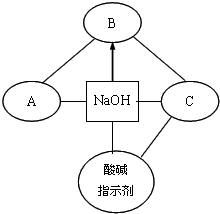
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com