
| A. | Mg | B. | Fe | C. | Cu | D. | Na |
分析 常温下,铝、铁和浓硝酸、浓硫酸易发生氧化还原反应而产生钝化现象,据此分析解答.
解答 解:A.常温下,镁和浓硫酸、浓硝酸反应生成盐及氧化物,故A不选;
B.常温下,铁和冷的浓硫酸、浓硝酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象称为钝化现象,故B选;
C.常温下,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,在加热条件下,铜和浓硫酸反应生成硫酸铜、二氧化硫和水,故C不选;
D.常温下,钠和冷、浓的硝酸或硫酸反应,不能形成致密氧化膜,故D不选;
故选B.
点评 本题考查了钝化现象的判断,明确钝化现象的内涵是解本题关键,根据铝、铁和冷的浓硝酸、浓硫酸的钝化现象用铝制或铁制容器运输浓硫酸、浓硝酸,注意:钝化现象不是金属和酸之间不反应,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶液中c(OH-)减小 | B. | pH的变化值等于2 | ||
| C. | 溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$的值增大 | D. | Kw的值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
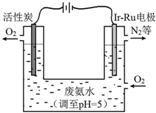 过氧化氢(H2O2)是淡蓝色的黏稠液体,水溶液为无色透明液体,俗称双氧水,可以看作二元弱酸.
过氧化氢(H2O2)是淡蓝色的黏稠液体,水溶液为无色透明液体,俗称双氧水,可以看作二元弱酸.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| C. | 钠加入水中:Na+H2O═Na++OH-+H2↑ | |
| D. | 铜片放入浓HNO3溶液中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
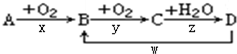
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

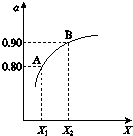

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量:g/mol | B. | 气体摩尔体积:mol/L | ||
| C. | 溶解度:g/100gH2O | D. | 密度:g/cm3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com