
某化学小组进行Na2SO3的性质实验探究。
在白色点滴板的a、b、c三个凹槽中滴有Na2SO3溶液,再分别滴加下图所示的试剂:
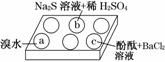
实验现象如下表:
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
根据实验现象进行分析:
(1)a中实验现象证明Na2SO3具有________性。
(2)b中发生反应的离子方程式是_____________________________________________
(3)应用化学平衡原理解释c中现象(用化学用语及简单文字表述)_______________
________________________________________________________________________。
解析:(1)a中发生反应的化学 方程式为:Na2SO3+Br2+H2O===Na2SO4+2HBr,证明Na2SO3具有还原性。
方程式为:Na2SO3+Br2+H2O===Na2SO4+2HBr,证明Na2SO3具有还原性。
(2)b中产生淡黄色沉淀,发生反应的离子方程式是SO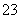 +2S2-+6H+===3S↓+3H2O。
+2S2-+6H+===3S↓+3H2O。
(3)滴入酚酞溶液变红是因为SO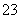 发生了水解反应而
发生了水解反应而 使溶液显碱性:SO
使溶液显碱性:SO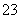 +H2OHSO
+H2OHSO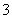 +OH-,再加入BaCl2溶液后,Ba2+与SO
+OH-,再加入BaCl2溶液后,Ba2+与SO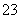 反应产生BaSO3沉淀,反应消耗了SO
反应产生BaSO3沉淀,反应消耗了SO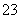 使其浓度减小,水解平衡向左移动,OH-浓度减小,红色褪去。
使其浓度减小,水解平衡向左移动,OH-浓度减小,红色褪去。
答案:(1)还原性 (2)SO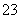 +2S2-+6H+===3S↓+3H2O
+2S2-+6H+===3S↓+3H2O
(3)在Na2SO3溶液中,SO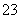 水解显碱性:SO
水解显碱性:SO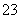 +H2OHSO
+H2OHSO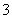 +OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO
+OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO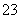 ===BaSO3↓(白色),由于c(SO
===BaSO3↓(白色),由于c(SO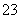 )减小,SO
)减小,SO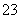 水解平衡左移,c(OH-)减小,红色褪去。
水解平衡左移,c(OH-)减小,红色褪去。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH = -57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH = 2×(-57.3)kJ·mol-1
B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g) =2CO(g)+O2(g)反应的 ΔH = 2×283.0 kJ·mol-1
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
关于反应中的先后顺序,下列评价正确的是( )
A.向浓度都为0.1 mol·L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应
B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH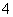 首先反应
首先反应
C.向浓度都为0.1 mol·L-1的FeCl3和CuCl2混合溶液中加入铁粉,FeCl3首先反应
D.向0.1 mol·L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应
查看答案和解析>>
科目:高中化学 来源: 题型:
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者的混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
(1)若假设1成立,则实验现象是_____________________________________________。
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?________。简述你的理由(不需写出反应方程式)____________
________________________________________________________________________。
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是________,写出发生反应的离子方程式________________________________。
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数,取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为________。
(5)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验室有下列试剂可供选择:A.氯水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
实验小组设计如下实验方案:
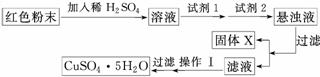

试回答:
①试剂1为________ (填字母,后同),试剂2为________。
(填字母,后同),试剂2为________。
②固体X的化学式为____________________________________________________。
③操作Ⅰ为___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②AlCl3、Al(OH)3 ③N2、NO ④S、SO2 ⑤NaOH、Na2CO3
A.①②⑤ B.②③⑤
C.③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列判断正确的是( )
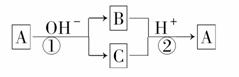
A.X元素可能为Al
B.X元素可能为Si
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24 mol B.0.16 mol
C.0.21 mol D.0.14 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
最近美国宇航员(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是
( )
A.分子中三个碳原子可能处在同一直线上
B.全氟丙烷的电子式为
C.相同压强下,沸点:C3F8<C3H8
D.全氟丙烷分子中既有极性键又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
甲酯除草醚(下图中E)是一种光合作用抑制剂,能被叶片吸收,但在植物体内传 导速度较慢,它是芽前除草剂,主要用于大豆除草。某烃A合成E的路线如下:A
导速度较慢,它是芽前除草剂,主要用于大豆除草。某烃A合成E的路线如下:A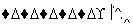
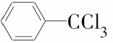
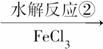
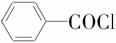
 B
B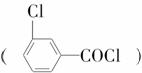

C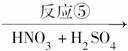 D
D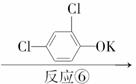
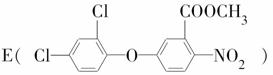
(1)写出A、C的结构简式:A________;C________。
(2)写出C中官能团的名称:________________。
(3)写出下列反应的化学方程式:
反应⑤_____________________________ _________________________;
_________________________;
反应⑥______________________ ____________________________________,
____________________________________,
反应类型是____________________________________________________。
(4)C的同分异构体有多种。写出核磁共振氢谱有四种不同化学环境的氢,且峰面积比为1∶2∶2∶2的四种有机物的结构简式: __________
______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com