
| A£® | ĻņNaHSO4ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗÖĮÖŠŠŌ£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O | |
| B£® | Ļņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČė×ćĮæCO2£ŗ2Na++CO32-+CO2+H2OØT2NaHCO3”ż | |
| C£® | ĻņCa£ØHCO3£©2ČÜŅŗÖŠ¼ÓČė×ćĮæCa£ØOH£©2ČÜŅŗ£ŗCa2++HCO3-+2OH-ØTCaCO3”ż+CO32-+2H2O | |
| D£® | Ļņ“ĪĀČĖįČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£ŗH++OH-ØTH2O |
·ÖĪö A£®ČÜŅŗĪŖÖŠŠŌŹ±£¬ĮņĖįĒāÄĘÓėĒāŃõ»Æ±µµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1£»
B£®Ģ¼ĖįĒāÄʵÄČܽā¶ČŠ”ÓŚĢ¼ĖįÄĘ£¬¶žÕß·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ³Įµķ£»
C£®ĒāŃõ»ÆøĘ×ćĮ棬·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĖ®£»
D£®“ĪĀČĖįĪŖČõĖį£¬Ąė×Ó·½³ĢŹ½ÖŠ“ĪĀČĖį²»ÄܲšæŖ£®
½ā“š ½ā£ŗA£®ĻņNaHSO4ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗÖĮÖŠŠŌ£¬ĒāĄė×ÓÓėĘóŅµ¹ćøęĄė×ÓĒ”ŗĆ·“Ó¦£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++2OH-+2H++SO42-ØTBaSO4”ż+2H2O£¬¹ŹA“ķĪó£»
B£®Ļņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČė×ćĮæCO2£¬·“Ӧɜ³ÉĢ¼ĖįĒāÄĘµÄ¹ż±„ŗĶČÜŅŗ£¬»įĪö³öĢ¼ĖįĒāÄĘ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Na++CO32-+CO2+H2OØT2NaHCO3”ż£¬¹ŹBÕżČ·£»
C£®ĻņCa£ØHCO3£©2ČÜŅŗÖŠ¼ÓČė×ćĮæCa£ØOH£©2ČÜŅŗ£¬Ģ¼ĖįøłĄė×Ó²»»įŹ£Óą£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCa2++HCO3-+OH-ØTCaCO3”ż+H2O£¬¹ŹC“ķĪó£»
D£®Ļņ“ĪĀČĖįČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£¬·“Ӧɜ³É“ĪĀČĖįÄĘŗĶĖ®£¬“ĪĀČĖįŠ”ÓŚ±£Įō·Ö×ÓŹ½£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗHClO+OH-ØTClO-+H2O£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖĄė×Ó·½³ĢŹ½µÄŹéŠ“ÅŠ¶Ļ£¬ĪŖøßæ¼µÄøßʵĢā£¬ŹōÓŚÖŠµČÄѶȵďŌĢā£¬×¢ŅāÕĘĪÕĄė×Ó·½³ĢŹ½ÕżĪóÅŠ¶Ļ³£ÓĆ·½·Ø£¬Čē£ŗ¼ģ²é·“Ó¦Īļ”¢Éś³ÉĪļŹĒ·ńÕżČ·£¬¼ģ²éø÷ĪļÖŹ²š·ÖŹĒ·ńÕżČ·£¬ČēÄŃČÜĪļ”¢Čõµē½āÖŹµČŠčŅŖ±£Įō»ÆѧŹ½£¬¼ģ²éŹĒ·ń·ūŗĻŌ»Æѧ·½³ĢŹ½µČ£®


 Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄĪļÖŹµÄĮæ/mol | ||||
| 0min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
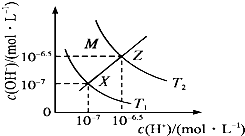
| A£® | ÓÉX”śZ£¬c£ØOH-£©Ōö“ó£¬ĖłŅŌæÉŅŌĶعż¼Ó¼īĄ“ŹµĻÖ | |
| B£® | MĒųÓņÄŚČĪŅāµć¾łÓŠc£ØH+£©£¼c£ØOH-£© | |
| C£® | T1ÓėT2Į½ĢõĒśĻßÖ®¼äµÄČĪŅāµć¾łÓŠc£ØH+£©”Įc£ØOH-£©=10-14 | |
| D£® | XZĻß±ķŹ¾c£ØH+£©=c£ØOH-£©£¬ČÜŅŗĻŌÖŠŠŌ£¬ĖłŅŌXZĻßÉĻČĪŅāµć¾łÓŠpH=7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
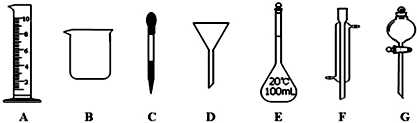
| A£® | ½šŹōÄĘ×Å»šŹ±Ź¹ÓĆÅŻÄĆš»šĘ÷Ćš»š | |
| B£® | ¼ÓČČĢ¼ĖįĒāÄĘ¹ĢĢåŹ±£¬ŹŌ¹Ü¹ÜæŚĒ抱ĻņÉĻ | |
| C£® | ŹµŃéŹŅÖĘČ”ĀČĘųŹ±£¬ÓĆNaOHČÜŅŗ½ųŠŠĪ²ĘųĪüŹÕ | |
| D£® | ÅØĮņĖį½¦µ½Ę¤·ōÉĻŹ±Į¢¼“ÓĆĻ”ĒāŃõ»ÆÄĘČÜŅŗ³åĻ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5£ŗ3 | B£® | 4£ŗ3 | C£® | 3£ŗ4 | D£® | 3£ŗ5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
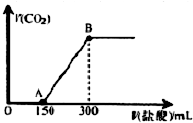 ¢ń”¢Čē¹ūÅäÖĘ3mol/LµÄNaOHČÜŅŗ500mL£¬Šč³ĘĮæNaOH¹ĢĢå60.0g£®
¢ń”¢Čē¹ūÅäÖĘ3mol/LµÄNaOHČÜŅŗ500mL£¬Šč³ĘĮæNaOH¹ĢĢå60.0g£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °×“×ÖŠµĪČėŹÆČļČÜŅŗ³ŹŗģÉ« | |
| B£® | °×“×¼ÓČė¶¹½¬ÖŠÓŠ³Įµķ²śÉś | |
| C£® | µ°æĒ½žÅŻŌŚ°×“×ÖŠÓŠĘųĢå·Å³ö | |
| D£® | ²āµĆ°×“×ČÜŅŗÖŠµÄc£ØH+£©ŌŚ1”Į10-2 mol•L-1µ½1”Į10-3 mol•L-1Ö®¼ä |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com