
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制城法”生产纯碱和化肥NH4Cl.工艺流程如图所示。下列有关说法不正确的是

A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 粗盐可采用除杂和重结晶等过程提纯
C. 流程图中的系列操作中用到的玻璃仪器可能有玻璃棒、烧杯、漏斗、坩埚等
D. 该流程中得到的晶体用到了溶解度的差异性
 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
【题目】某芳香烃X是一种重要的有机化工原料,分子式C7H8 . 现以它为初始原料设计出如图转化关系图(部分产物、合成路线、反应条件略去).其中A是一氯代物,F的分子式为C7H7NO2 , Y是一种功能高分子材料.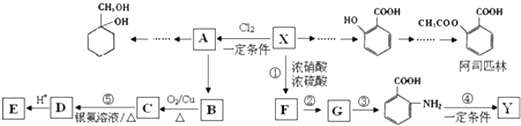
已知下列信息:
①烷基苯在高锰酸钾的作用下,侧链被氧化成羧基 ![]()
② ![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的结构简式是 , 其核磁共振氢谱图有个吸收峰;
(2)有机物C的结构简式是;
(3)阿司匹林分子中含有的官能团的名称是;1mol阿司匹林与足量NaOH溶液反应最多消耗NaOH的物质的量为mol;
(4)Y的结构简式为;
(5)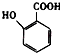 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有种;
(6)以下是由A和其他物质合成 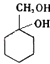 的流程:A
的流程:A ![]() 甲→乙
甲→乙 ![]()
![]()
![]()
![]() 甲→乙反应的化学方程式为 .
甲→乙反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下: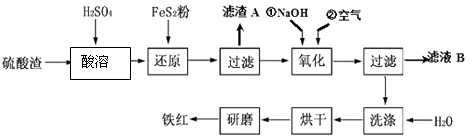
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为;“滤渣A”主要成份的化学式为 .
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+ , 而本身被氧化为H2SO4 , 请完成该反应的离子方程式:FeS2+14Fe3++H2O═15Fe2++SO ![]() + .
+ .
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 .
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式) .
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图所示.下列叙述正确的是( ) 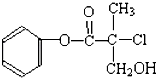
A.有机物A属于芳香烃
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热,可以发生消去反应
D.1mol A和足量的NaOH溶液反应,可以消耗3mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、(1) 4.9gH3PO4的物质的量为____,其中含有____molH,含有______个O,含磷元素___g,若它可与6gNa0H完全反应生成正盐,则H3PO4为_____元酸。
(2)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为____, 该金属元素为______。
II、有一包白色固体,可能含有CaCO3、Na2S04、KNO3、CuSO4、BaCl2五种物质中的一种或几种,现进行如下实验:
(1)取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
(2)继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
(3)取少量(2)中的溶液滴加Ba(NO3)2为溶液,有白色沉淀生成,加稀硝酸沉淀不溶。
根据上述实验现象判断:该白色固休中一定含有____,一定不含有____,可能含有_____。
III、小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.504gNaHCO3, 2片小苏打片和胃酸完全中和,被中和的H+是___mol。
(2)胃舒平每片含0.234gAl(OH)3。写出胃舒平中和胃酸的离子反应方程式___, 中和胃酸时,6片小苏打片相当于胃舒平_____片。
(3)达喜的化学成分是铝和镁的碱式盐。取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,则该碱式盐样品中氢氧根与碳酸根的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:

(1)写出上述实验过程中所用试剂:试剂①___________;试剂③___________。
(2)判断试剂①已过量的方法是:_______________________。
(3)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉__________(填“能”或“不能”)透过半透膜;SO42-___________(填“能”或“不能”)透过半透膜。
(4)操作④的名称是________________。
(5)实验室用制得的NaCl晶体配制480mL1.0mol/L的NaCl溶液,用托盘天平称量的氯化钠固体的质量是___________,配制过程用到的玻璃仪器除量筒、烧杯、胶头滴管外,还有_____________。
(6)分析以下操作对配制的溶液浓度造成的影响,影响偏高的是____________________。
①蒸馏水洗完容量瓶后没有烘干
②转移溶液过程中出现漏液
③溶解后未经冷却就转移到容量瓶
④定容时俯视
⑤摇匀后发现液面降低,再加蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com