
将100mL 3mol·L-1的NaOH溶液与100mL 3mol·L-1的AlCl3溶液按下列两种方法混合:(1)将NaOH溶液逐滴滴入AlCl3溶液中 (2)将AlCl3溶液逐滴滴入NaOH溶液中,对上述实验所得结论正确的是
A.现象相同,沉淀量相等 B.现象相同,沉淀量不等
C.现象不同,沉淀量相等 D.现象不同,沉淀量不等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年河南省三门峡市高二6月月考化学试卷(解析版) 题型:选择题
不同的金属应选用不同的冶炼方法,如:热还原法、热分解法、电解法等。你认为选择的原则主要是依据( )
A.金属在自然界的存在形式
B.金属熔点的高低
C.金属离子得电子的能力
D.金属元素在地壳中的含量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一下学期5月月考化学试卷(解析版) 题型:选择题
a、b、c、d四个金属电极,有关的实验装置现象如表所示:由此判断这四个电极对应的金属活动性由强到弱的顺序为 ( )
装置 | CuSO4溶液 | 稀硫酸 | 稀硫酸 |
现象 | a极质量减小 b极质量增大 | b极有气泡 c极无明显现象 | 电流从a极流向d极 |
A.d>a>b>c B.b>c>d>a C.a>b>c>d D.a>b>d>c
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二6月月考化学试卷(解析版) 题型:选择题
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是

A.a点对应的溶液中:Na+、Fe3+、SO、HCO
B.b点对应的溶液中:Ag+、Ca2+、NO、F-
C.c点对应的溶液中:Na+、S2-、SO、Cl-
D.d点对应的溶液中:K+、NH、I-、CO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二6月月考化学试卷(解析版) 题型:选择题
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
A.2mol·L-1H2SO4溶液 B.18mol·L-1H2SO4溶液
C.6mol·L-1KOH溶液 D.3mol·L-1HNO3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二6月月考化学试卷(解析版) 题型:选择题
取ag某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了ag。下列物质中不能满足上述结果的是
A.H2 B.CO C.C6H12O6 D.C12H22O11
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下学期期中化学试卷(解析版) 题型:实验题
乙醇的沸点是78 ℃,能与水以任意比混溶,易与氯化钙结合生成配合物。乙醚的沸点为34.6 ℃,难溶于水,乙醚极易燃烧。实验室制乙醚的反应原理是:
2CH3CH2OH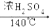 CH3CH2—O—CH2CH3 (乙醚)+H2O
CH3CH2—O—CH2CH3 (乙醚)+H2O
实验步骤:
Ⅰ.乙醚的制备
在分液漏斗中加入2 mL 95%的乙醇,在一干燥的三颈烧瓶中放入12 mL 95%的乙醇,在冷水浴中的冷却下边摇动边缓慢加入12 mL浓硫酸,使混合均匀,并加入2粒沸石。实验装置如下图:
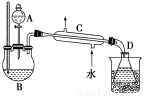
将反应瓶放在电热套上加热,使温度迅速地上升到140 ℃,开始由分液漏斗慢慢滴加乙醇,控制流速并保持温度在135~140 ℃之间。待乙醇加完后,继续反应10 min,直到温度上升到160 ℃止。关闭热源,停止反应。
Ⅱ.乙醚的精制
将馏出物倒入分液漏斗中,依次用8 mL 15% NaOH溶液、8 mL饱和食盐水洗涤,最后再用8 mL饱和氯化钙溶液洗涤2次,充分静置后分液。将乙醚倒入干燥的锥形瓶中,用块状无水氯化钙干燥。待乙醚干燥后,加入到蒸馏装置中用热水浴蒸馏,收集33~38 ℃的馏分。
请根据上述信息,完成下列问题:
(1)乙醚的制备和精制过程中都需要使用沸石,其作用是________________________,
如果实验中忘记加沸石,需要怎么处理?______________________________________。
(2)乙醚的制备和精制过程中都需要使用温度计,其水银球位置是否相同?________(填“是”或“否”),原因是_____________________________________________________________。
(3)仪器C的名称为________。
(4)如果温度太高,将会发生副反应,产物是__________。
(5)精制乙醚中,加入15% NaOH溶液的作用是_________,加入饱和氯化钙溶液的作用是_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏高一下学期期中考试化学试卷(解析版) 题型:选择题
用过量的锌与稀硫酸反应制H2时,下列能减缓反应速率但又不影响生成氢气总量的是( )
A. 加入少量Na2CO3固体 B. 加入少量CuSO4溶液
C. 加入少量NaOH固体 D. 加水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:实验题
乙醛在氧化铜催化下,可以被空气氧化成乙酸。依据此原理设计验证实验(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水用于收集少量乙酸溶液;烧杯B中装有某液体)。已知在60℃~80℃时,用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:

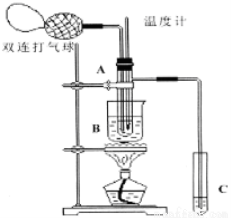
请回答下列问题:
(1)试管A内在60~80℃时发生的主要反应的化学方程式为(注明反应条件) ;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在 ;目的是 ;当试管A内的主要反应完成后温度计水银球的位置应在 ,目的是 ;
(3)烧杯B的作用是 ;烧杯B内盛装的液体可以是 或 (在上表中物质里选择,填写结构简式);
(4)若想检验试管C中是否含有产物乙酸,请你在下列药品中进行选择,设计一个简便的实验方法。可供选择的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方法为________ ;
(5)已知乙醛能被溴水氧化,写出该反应的化学方程式______________________________ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com