
����Ŀ��������ʵ����ʵ���������������Ӧ������ȷ���ǣ� ��
ѡ�� | ʵ����ʵ����� | ���� |
A | ����������ͬ�� | ��������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ� |
B | �ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı� | ����һ�������뻯ѧ��Ӧ |
C | ���ʵ���Ũ����ͬ������ʹ���ֱ������������״��ͬ��п����Ӧ | ��ʼʱ�ķ�Ӧ������ͬ |
D | ���ݻ��ɱ���ܱ������з�����Ӧ | ����Ӧ���ʼӿ죬�淴Ӧ���ʲ��� |
A. AB. BC. CD. D
���𰸡�A
��������
A��![]() �Ƿ�Ӧ�����������ͬ��
�Ƿ�Ӧ�����������ͬ��![]() ��ҺŨ��Խ���������������ʱ��Խ�̣�˵��������������ʱ������Ӧ��Ũ�ȣ���ѧ��Ӧ���ʼӿ죬ѡ��A��ȷ��
��ҺŨ��Խ���������������ʱ��Խ�̣�˵��������������ʱ������Ӧ��Ũ�ȣ���ѧ��Ӧ���ʼӿ죬ѡ��A��ȷ��
B���������뻯ѧ��Ӧ���ı��˷�ӳ��;��������Ӧǰ���������ͻ�ѧ���ʶ����䣬ѡ��B����
C������������״��ͬ�Ľ������ᷴӦʱ��������Ũ����ͬ����������ͬ����Ϊ����ʹ������ʵ���Ũ����ͬ�������������ᣬ��ˮ��Һ�в�����ȫ���룬���Կ�ʼʱ������Ũ�Ȳ�ͬ����ʼʱ��Ӧ���ʲ�ͬ��ѡ��C����
D���ݻ���Сһ�룬ѹǿ���������淴Ӧ���ʾ��ӿ죬ѡ��D����
��ѡA��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(G)��һ����Ҫ������һ�ֺϳɇ����·����ͼ��ʾ��
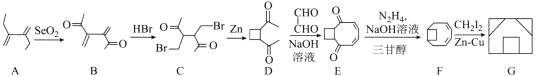
��֪��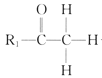 +R2��CHO
+R2��CHO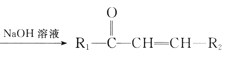 +H2O��
+H2O��
��ش��������⣺
��1��A�Ļ�ѧ����Ϊ___��G�ķ���ʽΪ__��
��2��B��C�ķ�Ӧ����Ϊ___��C�����������ŵ�����Ϊ__��
��3��D��E�Ļ�ѧ����ʽΪ___��
��4��ͬʱ��������������B��ͬ���칹����__��(�����������칹)�����к˴Ź���������5���Ľṹ��ʽΪ___��
�����ڷ����廯�����ұ���������3��ȡ������
����FeC13��Һ������ɫ��Ӧ��
��5�����������ϳ�·�ߺ���Ϣ����![]() Ϊԭ��(�����Լ���ѡ)������Ʊ�
Ϊԭ��(�����Լ���ѡ)������Ʊ�![]() �ĺϳ�·�ߣ�___��
�ĺϳ�·�ߣ�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Դ����������Ч����CO2�ŷţ��������̼��Դ��
��1��CaO���ڽϸ��¶��²���CO2���ڸ����¶��½�������CO2�ͷ����á�CaC2O4��H2O�ȷֽ���Ʊ�CaO��CaC2O4��H2O�������¹����й���������仯����ͼ��

��д��400~600 �淶Χ�ڷֽⷴӦ�Ļ�ѧ����ʽ��________��
����CaCO3�ȷֽ��Ʊ���CaO��ȣ�CaC2O4��H2O�ȷֽ��Ʊ���CaO���и��õ�CO2�������ܣ���ԭ����________��
��2����ⷨת��CO2��ʵ��CO2��Դ�����á����CO2��HCOOH��ԭ��ʾ��ͼ���¡�

��д������CO2��ԭΪHCOO�ĵ缫��Ӧʽ��________��
�ڵ��һ��ʱ�����������KHCO3��ҺŨ�Ƚ��ͣ���ԭ����________��
��3��CO2������ϳɶ�������һ��CO2ת�����������������Ҫ�������з�Ӧ��
��Ӧ��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H =41.2 kJ��mol1
CO(g)+H2O(g) ��H =41.2 kJ��mol1
��Ӧ��2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ��H =��122.5 kJ��mol1
CH3OCH3(g)+3H2O(g) ��H =��122.5 kJ��mol1
�ں�ѹ��CO2��H2����ʼ��һ���������£�CO2ƽ��ת���ʺ�ƽ��ʱCH3OCH3��ѡ�������¶ȵı仯��ͼ�����У�

CH3OCH3��ѡ����=![]() ��100��
��100��
���¶ȸ���300 �棬CO2ƽ��ת�������¶����߶�������ԭ����________��
��220 ��ʱ���ڴ���������CO2��H2��Ӧһ��ʱ����CH3OCH3��ѡ����Ϊ48%��ͼ��A�㣩�����ı䷴Ӧʱ����¶ȣ�һ�������CH3OCH3ѡ���ԵĴ�ʩ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2 L���ܱ������У�����1mol X(g)��2 mol Y(g)������Ӧ��X(g)��mY(g)![]() 3Z(g) ��H��0��ƽ��ʱ��X��Y��ת���ʶ���10%��������������ȷ����
3Z(g) ��H��0��ƽ��ʱ��X��Y��ת���ʶ���10%��������������ȷ����
A��m=2
B����ƽ��ʱ��Z���������Ϊ10%
C����ƽ���������������䣬���ȣ�������ѹǿ������
D����ƽ�����������ѹ����1L��X��Ũ��Ϊ0.45mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���о������ص����ʡ���������ͨ�����������Ƶ�ԭ�ӽṹʾ��ͼ�������й����ϣ�֪������������ͬһ�����ʣ�������������������֮�������ڽ������˳����У��������Ƶ�ǰ�棬���ڿ�����ȼ�յIJ����dz�������(KO2)��
(1)Ԥ��صĻ�ѧ���ʣ�������з�Ӧ�Ļ�ѧ����ʽ��
�ټ���������ȼ��____________________________��
�ڵ�ȼ�ؾ���ȼ��_____________________________��
�۽�С���Ͷ����ˮ��______________________________��
(2)�Ʋ������Ȼ���еĴ��ڷ�ʽ��(��������̬����������̬��)________��
(3)��С���о��ص�����ʱ�õ�����Ҫ������____________________________________��
(4)�����о����������ʵij�����__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ�����ƣ����岽�����£�
![]()
��ʱ����õ�ʵ������ͼ���£�
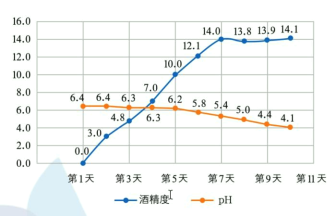
����˵������ȷ����
A.Ŵ���е����ھ������ǻ�ø������ˮ��Ϊ�����ǣ��������ھƻ�ø������ת��Ϊ�Ҵ�
B.����������� pH ���½�����������Ϊ�����Ҵ�����������Ϊ����
C.�ӵ� 7 �쿪ʼ�Ƶľƾ��Ƚ������䣬˵����Һ�е��������Ѿ���ȫ��Ӧ
D.��С������������ƾƾ��Ȳ��ߣ��ɲ���������߾ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 0.1000 mol��L1 NaOH ��Һ�ֱ�ζ� 20.00 mL 0.1000 mol��L1 ������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����
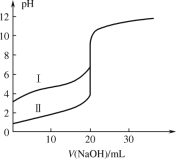
A.�������ֱ��ʾ����ʹ���ĵζ�����
B.V(NaOH) = 10.00 mL ʱ��������Һ��c(CH3COOH)��c(CH3COO)
C.pH = 7 ʱ���ζ��������ĵ� NaOH ��Һ���С�ڵζ��������ĵ� NaOH ��Һ���
D.V(NaOH) = 20.00 mL ʱ������Һ�� c(CH3COO)��c(Cl)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�����H2A��Һ�У�����H2A��HA����A2��������̬�����ӣ������ʵ���������[��(X)��![]() ]����ҺpH�仯�Ĺ�ϵ��ͼ��ʾ������˵���������
]����ҺpH�仯�Ĺ�ϵ��ͼ��ʾ������˵���������
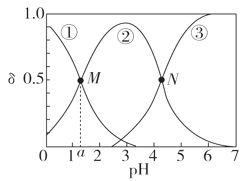
A.pH>4����Һ�У���(A2��)��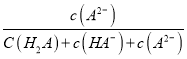 ��
��
B.M���Ӧ����Һ��ˮ�ĵ���̶�С��N��
C.��ͼ��aΪ1.2����lg [Ka1(H2A)]����1.2
D.���ߢڴ�����������HA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ���ڼӳɷ�Ӧ����
A.CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
B.CH2=CH2+HCl![]() CH3CH2Cl
CH3CH2Cl
C.CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
D.2C6H6 + 15O2![]() 12CO2 +6H2O
12CO2 +6H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com