
| A. | SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 | |
| B. | SO2是硫在空气中不完全燃烧的产物,SO3是硫在空气中完全燃烧的产物 | |
| C. | 大气中SO2的主要来源是汽车排出的尾气 | |
| D. | SO2具有漂白性,因而可以使石蕊试液褪色 |
分析 二氧化硫为无色、刺激性气味的有毒气体,与水反应,且具有漂白性,S元素化合价为+4价,处于中间价态,即具有氧化性也具有还原性,
A.二氧化硫中元素化合价+4价处于中间价态,可以升高也可以降低;
B.硫单质燃烧生成二氧化硫和用量无关;
C.汽车排出的尾气主要是氮氧化物、一氧化碳等;
D.SO2具有漂白性,能使品红褪色.
解答 解:A.S、H2S氧化可生成SO2,浓硫酸被还原也可生成SO2,故A正确;
B.硫单质在空气中燃烧只能生产二氧化硫,不能生成三氧化硫,故B错误;
C.二氧化硫主要来源含硫物质的燃烧,汽车尾气中主要含氮的氧化物、一氧化碳,故C错误;
D.SO2具有漂白性,能使品红褪色,但不能使石蕊试液褪色,遇石蕊试液变红,故D错误;
故选A.
点评 本题考查二氧化硫的性质、来源等知识点,二氧化硫具有氧化性、还原性和漂白性,易错选项是D,注意二氧化硫不能漂白酸碱指示剂,为易错点,题目较简单.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol•L-1氨水中有NA个NH4+ | |
| B. | 常温常压下,22.4 L CO2中含有NA个CO2分子 | |
| C. | 1L 0.1mol•L-1Na2SO3溶液中含有 0.1NA个SO32- | |
| D. | 1L 0.1mol•L-1AlCl3溶液中含有氯离子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
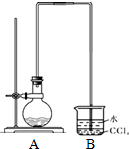 溴苯是一种常用的化工原料,通常情况下为无色油状液体,不溶于水,溶于多数有机溶剂.沸点156.2℃,较难挥发.某同学拟用如下装置制备溴苯(已检查气密性):
溴苯是一种常用的化工原料,通常情况下为无色油状液体,不溶于水,溶于多数有机溶剂.沸点156.2℃,较难挥发.某同学拟用如下装置制备溴苯(已检查气密性): .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 氯化钙溶液与碳酸钠溶液反应:Ca2++CO32-═CaCO3↓ | |
| C. | 硫酸溶液与碳酸钡反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的热稳定性依次减弱 | |
| B. | 水结成冰体积膨胀,密度变小 | |
| C. | NH3易液化 | |
| D. | 在相同条件下,H2O的沸点比H2S的沸点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
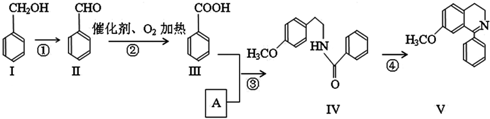
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2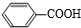
 +
+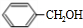 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O
+H2O
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com