
| A、胶体 | B、悬浊液 |
| C、溶液 | D、乳浊液 |
科目:高中化学 来源: 题型:
| A、点燃可燃性气体前验纯 |
| B、气体实验装置在实验前进行气密性检查 |
| C、胶头滴管不能交叉使用 |
| D、实验剩余的药品不能放回原试剂瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、30g甲醛(HCHO)和醋酸的混合物中含碳原子数目为NA |
| B、1mol Cl2与足量的NaOH溶液反应,转移的电子数为2NA |
| C、100mL0.2mol?L-1的AlCl3溶液中,含Al3+数为0.02NA |
| D、电解精炼铜时,阳极减少6.4g,则转移电子数一定是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、①③④ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
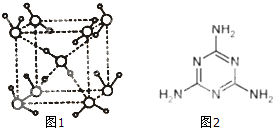 聚合铁(简称PFS)化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10.现代污水处理工艺中常利用PFS在水体中形成絮状物,以吸附重金属离子.
聚合铁(简称PFS)化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10.现代污水处理工艺中常利用PFS在水体中形成絮状物,以吸附重金属离子.查看答案和解析>>
科目:高中化学 来源: 题型:
| O2 |
| 800℃ |
| O2 |
| △① |
| Cu2S |
| △② |
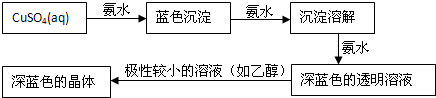
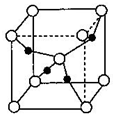
查看答案和解析>>
科目:高中化学 来源: 题型:
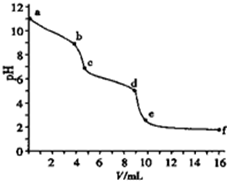
| A、以酚酞为指示剂,溶液颜色发生突变时(b点),Na2CO3转化为NaHCO3 |
| B、以甲基橙为指示剂,溶液颜色发生突变时,共消耗盐酸20.00ml |
| C、溶液pH=7(c点),碳酸钠完全转化为NaCl |
| D、ce段对应溶液中CO2与NaHCO3共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com