
分析 (1)反应中化合价降低的元素被还原;
(2)冶炼过程产生大量SO2,处理方案中合理的分析是二氧化硫是污染性气体,不能排放到空气中,可以吸收利用;
(3)过二硫酸钾(K2S2O8)、三价铁离子均具有强氧化性,碘离子具有还原性,根据氧化剂和还原剂的性质以及题意信息来回答;
(4)a、氧化铝是两性氧化物,能和强酸以及强碱反应,利用氢氧化钠使其变为偏铝酸根即可;
b、证明含有Fe2O3,需要加酸溶解,然后检验铁离子;亚铁离子能被高锰酸钾溶液氧化,使的高锰酸钾溶液褪色.
解答 解:(1)化合价降低的元素Cu、O,在反应中被还原,故答案为:Cu、O;
(2)a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理,故a错误;
b.可以利用吸收二氧化硫生成硫酸,用于制备硫酸,故b合理;
c.用纯碱溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用浓硫酸不能吸收二氧化硫,故d不合理;
故答案为:b、c;
(3)根据题意过二硫酸钾(K2S2O8)、三价铁离子均具有强氧化性,碘离子具有还原性,通过改变反应途径,Fe2+均可催化反应S2O82-+2I-=2SO42-+I2;实质是:2Fe3++2I-=2Fe2++I2,S2O82-+2Fe2+=2SO42-+2Fe3+,
故答案为:2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;
(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++Al2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成偏铝酸根,
故答案为:Al3++4OH-=2H2O+AlO2-;
b.证明含有Fe2O3,需要加酸溶解,然后检验铁离子,所以需要稀硫酸和KSCN溶液,检验亚铁离子要利用亚铁离子的还原性,高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,
故答案为:稀硫酸、KSCN溶液、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色.
点评 本题考查了硫元素及其化合物的性质,题目难度中等,题目涉及元素化合物的性质、氧化还原反应、离子方程式的书写、物质的检验等,侧重于考查学生对基础知识的综合应用能力.


科目:高中化学 来源: 题型:选择题
| 弱酸 | 电离常数 |
| CH3COOH | K=1.75×10-5 |
| H2CO3 | K1=4.4×10-7 k2=4.7×10-11 |
| HClO | K=3.2×10-8 |
| A. | ②>④>③>① | B. | ①>③>④>② | C. | ③>②>④>① | D. | ③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核外电子排布--元素在周期表中的位置 | |
| B. | 弱电解质的相对强弱--电离常数的大小 | |
| C. | 分子间作用力的大小--分子稳定性的高低 | |
| D. | 物质内部储存的能量--化学反应的热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应过程中的氧化产物均为SO3 | |
| B. | a点时消耗NaHSO3的物质的量为1.0 mol | |
| C. | 0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ | |
| D. | 当溶液中I?与I2的物质的量之比为1:1时,加入的NaIO3为1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性 | B. | 还原性 | ||
| C. | 既无氧化性又无还原性 | D. | 既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
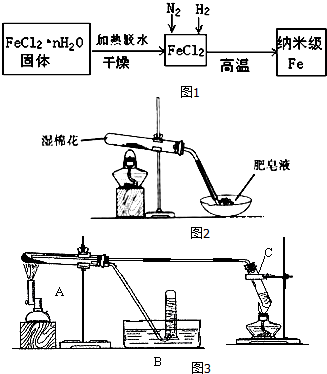
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| Ⅱ | 向实验I中得到的溶液滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属铝溶于氢氧化钠溶液:Al+2OH-═2AlO2-+H2↑ | |
| B. | NaHCO3溶液与硫酸氢钠溶液混合:HCO3-+H+═H2O+CO2↑ | |
| C. | 过氧化钠与水反应:Na2O2+2H2O═2Na++2OH-+O2↑ | |
| D. | Ca(OH)2溶液中通入过量CO2:Ca2++2OH-+CO2═CaCO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com