
【题目】下列说法正确的是( )。
A.已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液中
CH3COO-+H+,加少量烧碱溶液可使溶液中![]() 值增大
值增大
B.25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O![]() H++OH-逆向移动,c(H+)降低
H++OH-逆向移动,c(H+)降低
C.取c(H+)=0.01 mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.3 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3- )
【答案】AC
【解析】
A.加入烧碱,氢氧根离子和氢离子反应,导致溶液中氢离子浓度减小,平衡正向移动,![]() 值增大,故A正确;
值增大,故A正确;
B.含有弱离子的盐能够水解,促进水的电离,向水中加入醋酸钠固体,醋酸根离子水解,是结合氢离子生成了弱电解质醋酸,溶液中氢离子浓度减小,促进水的电离,故B错误;
C.反应速率与氢离子浓度成正比,c(H+)=0.01molL-1的盐酸和醋酸,醋酸浓度大于盐酸,加水稀释促进醋酸电离,导致醋酸中氢离子浓度大于盐酸,所以醋酸反应速率大,故C正确;
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液,溶液中存在物料守恒,根据物料守恒得c(Na+)=c(NO3-),故D错误;
故选AC。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某可逆反应在某体积为5L的密闭容器中进行,在从0~3分钟各物质的量的变化情况如图所示(A、B、C均为气体)
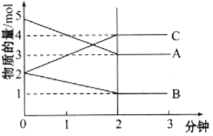
(1)该反应的化学方程式为__________________。
(2)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是___________(填字母)。
A.气体总质量保持不变 B.A、B、C的浓度都相等
C.A、B、C的浓度不再发生变化 D.A、B、C的分子数之比为2:1:2
E.正反应和逆反应都已停止 F.容器内气体密度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,其中可能含NH4+、K+、Na+、Mg2+、H+、Cu2+、CO32-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,发现溶液呈强酸性。
②取部分溶液,逐滴加入NaOH稀溶液,使溶液逐渐从酸性转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成。
③将②得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答下列问题:
(1)在溶液中,肯定存在的离子有________,肯定不存在的离子有________,不能确定是否存在的离子有________。
(2)写出实验③中的离子方程式:___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中的实验方案,能达到实验目的的是 ( )
A.验证FeCl3对H2O2分解反应有催化作用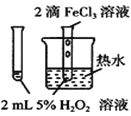
B.探究温度对平衡2NO2![]() N2O4的影响
N2O4的影响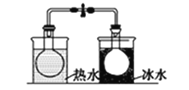
C.除去CO2气体中混有的SO2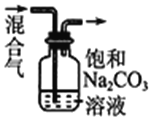
D.比较HCl、H2CO3和H2SiO3的酸性强弱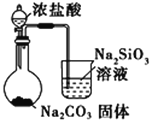
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。下列推断正确的是 ( )

A.a极应与电源的负极相连
B.膜1为阴离子交换膜,膜2为阳离子交换膜
C.a极的电极反应式为2H2O一4e一=4H++O2↑
D.若收集22.4L的P(标准状况下),则转移4mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是![]()
![]()
A.常温下,![]() 的甲酸溶液的
的甲酸溶液的![]() 与
与![]() 的氨水溶液中由水电离产生的
的氨水溶液中由水电离产生的![]() 相等
相等
B.中和 ![]() 醋酸与中和
醋酸与中和 ![]() 的醋酸所需同种碱溶液的物质的量不同
的醋酸所需同种碱溶液的物质的量不同
C.向![]() 溶液中逐渐加入适量NaOH固体,溶液的导电性明显增强
溶液中逐渐加入适量NaOH固体,溶液的导电性明显增强
D.向饱和石灰水中加入少量CaO,恢复至室温后溶液中![]() 增大,导电能力增强
增大,导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )

A. ①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度(acidity grade),AG的定义为AG = lg[![]() ].室温下实验室中用0.01molL-1的氢氧化钠溶液滴定20.00mL 0.01molL-1的一元弱酸HA,滴定过程如图所示,下列叙述正确的是( )
].室温下实验室中用0.01molL-1的氢氧化钠溶液滴定20.00mL 0.01molL-1的一元弱酸HA,滴定过程如图所示,下列叙述正确的是( )

A. 室温下,弱酸HA的电离常数约为10-5
B. A点时加入氢氧化钠溶液的体积为20.00mL
C. 若B点为40mL,所得溶液中:c(OH-) = c(A-)+c(HA)+c(H+)
D. 反应过程中一定存在:0.01molL-1+c(OH-)=c(Na+)+c(HA)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com