

���� AΪ����ɫ���壬��A�ܺ�ˮ��Ӧ������ɫ��ζ����C����A��Na2O2����C��O2��B��NaOH��D�Ǿ��д��Եĺ�ɫ���壬��D��Fe3O4������T��������ȼ��������������������T��Fe�����������������������ᡢ������Fe��Ӧ�õ�E��E��B��NaOH����Ӧ�õ���ɫ����H����EΪFeCl2��H��Fe��OH��2��H�ڳ�ʪ�Ŀ����еõ�MΪFe��OH��3��M��HCl��Ӧ����W����W��FeCl3������R��������Ӧ����������Q��Q�ܺ�NaOH��Һ��Ӧ����R��Al��Q��Al2O3��N��NaAlO2���ݴ˽��
��� �⣺AΪ����ɫ���壬��A�ܺ�ˮ��Ӧ������ɫ��ζ����C����A��Na2O2����C��O2��B��NaOH��D�Ǿ��д��Եĺ�ɫ���壬��D��Fe3O4������T��������ȼ��������������������T��Fe�����������������������ᡢ������Fe��Ӧ�õ�E��E��B��NaOH����Ӧ�õ���ɫ����H����EΪFeCl2��H��Fe��OH��2��H�ڳ�ʪ�Ŀ����еõ�MΪFe��OH��3��M��HCl��Ӧ����W����W��FeCl3������R��������Ӧ����������Q��Q�ܺ�NaOH��Һ��Ӧ����R��Al��Q��Al2O3��N��NaAlO2��
��1��ͨ�����Ϸ���֪��A��Na2O2��D��Fe3O4���ʴ�Ϊ��Na2O2��Fe3O4��
��2��NaOH��FeCl2��͵õ�Fe��OH��2���ڳ�ʪ�����б��Fe��OH��3�Ĺ����У����ܹ۲쵽��������Һ�г��ְ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ����Ӧ����ʽΪ��4Fe��OH��3+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ����Һ�г��ְ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��4Fe��OH��3+O2+2H2O=4Fe��OH��3��
��3��B��R��Ӧ����N�����ӷ���ʽΪ��2Al+2OH-+2H2O�T2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O�T2AlO2-+3H2����
���� ���⿼�������ƶϣ��漰Na��Al��Fe��Ԫ�ص��ʻ�����������ת�������ʵ���ɫ��ת����ϵ�������ⷴӦ���ƶ�ͻ�ƿڣ���Ҫѧ�����������������ʣ���Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��1 | C�� | 3��4 | D�� | 5��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ú��ˮú�����Ƕ�����Դ | |
| B�� | ú�к��б����ױ������ױ����л��� | |
| C�� | ���ǽ�ú�ڿ����м�ǿ��ʹ��ֽ�Ĺ��� | |
| D�� | BΪ�״�������ʱ��ԭ�������ʾ��ﵽ100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��APEC������2014���µ�����ʻ㣬����2014��APEC�����ڼ䱱����������գ�˵������ʵʩ��·���к���Ⱦ��ҵͣ���ȴ�ʩ���Լ�����������֤������������Ч�� | |
| B�� | ���ع��͡������ӹ��������������Ʒ������������ | |
| C�� | ��ʯ�ҡ����ۡ��轺��ʳƷ��װ�г��õĸ���� | |
| D�� | ����������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
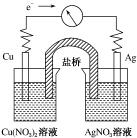 ����ӦCu��s��+2Ag+��aq���TCu2+��aq��+2Ag��s����Ƴ�ԭ��أ�ijһʱ�̵ĵ����������ƣ�G��ָ��ƫת������ͼ��ʾ�������й�������ȷ���ǣ�������
����ӦCu��s��+2Ag+��aq���TCu2+��aq��+2Ag��s����Ƴ�ԭ��أ�ijһʱ�̵ĵ����������ƣ�G��ָ��ƫת������ͼ��ʾ�������й�������ȷ���ǣ�������| A�� | KNO3�����е�K+����Cu��NO3��2��Һ | |
| B�� | Cu��������������ԭ��Ӧ | |
| C�� | ������AgNO3��Һͨ����������Cu��NO3��2��Һ | |
| D�� | ����һ��ʱ���AgNO3��Һ��c��Ag+����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18g��ˮ��D2O���к���10NA������ | |
| B�� | 22.4Lһ�ȼ���ķ�����ԼΪNA | |
| C�� | 4.6g Na����������ȫ��Ӧ����Na2O��Na2O2��ת�Ƶ�����Ϊ0.2NA | |
| D�� | 25��ʱ��1L pH=14��Ba��OH��2��Һ�У�Ba2+��ĿΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com