
【题目】在一定条件下xA+yB![]() zC达到平衡时,请填写:
zC达到平衡时,请填写:
(1)若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是______________。
(2)已知B、C是气体,现增加A的物质的量,平衡不移动,说明A是_____________(填状态)。
(3)若容器容积不变,加入气体B,气体A的转化率__________(填“增大”“减小”或“不变”)。
(4)若加热后,C的百分含量减小,则正反应是___________反应(填“放热”或“吸热”)。
(5)若容器容积不变,且A、B、C都是气体,向容器中充入稀有气体,则 。
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不移动 D.反应停止
【答案】(1)x+y﹥z;(2)固体或液体;(3)增大 ;(4)放热 ;(5)C;
【解析】
试题分析:在一定条件下xA+yB![]() zC达到平衡时,(1)当其他条件不变时,减小压强平衡向气体物质的量增大的方向移动。若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是x+y﹥z。
zC达到平衡时,(1)当其他条件不变时,减小压强平衡向气体物质的量增大的方向移动。若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是x+y﹥z。
(2)增加固体或纯液体的用量对化学反应速率几乎无影响。现增加A的物质的量,平衡不移动,说明A是固体或液体。
(3)若容器容积不变,加入气体B,平衡正向移动,气体A的转化率增大。
(4)当其他条件不变时,升高温度,平衡向吸热反应方向移动。若加热后,C的百分含量减小,平衡逆向移动,则正反应是放热反应。
(5)若容器容积不变,且A、B、C都是气体,向容器中充入稀有气体,与反应相关的各物质的浓度不变,化学反应速率不变,化学平衡不移动,选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有以下几种物质:①NH3②Na2CO3固体③C2H5OH(乙醇)④盐酸⑤Cu⑥NaCl晶体⑦Fe(OH)3胶体填空回答:
(1)以上物质属于电解质的有 (填编号,下同),属于非电解质的有 。
(2)②既是钠盐又是碳酸盐,对该物质的分类方法是 。
(3)实验室制备⑦的化学方程式为 。
证明有⑦生成的实验操作及现象是 。
NaCl晶体溶解在 (填以上物质序号)中也有此现象。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S都是重要的非金属元素。下列说法正确的是( )
A. 三者对应的氧化物均为酸性氧化物
B. 实验室可用NaOH溶液处理SO2、NO2
C. CO2、NO2、SO2都能与H2O反应,其反应原理相同
D. 三者的单质直接与氧气反应都能生成两种氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】模拟电渗析法将海水淡化的工作原理示意图如下。己知X、Y均为惰性电极,模拟海水中富含Na+、Cl—、Ca2+、Mg2+、SO42—等离子。下列叙述中不正确的是

A.N是阴离子交换膜
B.Y电极上产生有色气体
C.X电极区域有浑浊产生
D.X电极反应式为4OH——4e—=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组实验:①除去混在植物油中的水②回收碘的CCl4溶液中的CCl4③用食用酒精浸泡中草药提取其中的有效成分。分离以上混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质.为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按图所示步骤进行操作.

回答下列问题:
(1)为检验起始滤液中的Cl﹣,所用试剂除了稀HNO3,还需要 ;
(2)试剂I的化学式为 ,判断试剂I已加过量的方法 ;
(3)试剂Ⅱ的化学式为 ②中加入试剂Ⅱ的目的是 ;
(4)试剂Ⅲ的名称是 ③中发生反应的离子方程式为 ;
(5)某同学根据最终所得KCl晶体质量和原样品的质量算出氯化钾样品的纯度,你认为结果可靠吗?并说明理由(不考虑实验误差)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)该浓盐酸中HCl的物质的量浓度为 molL-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.400 molL-1的稀盐酸。
①容量瓶上需标有以下五项中的
A温度 B浓度 C容量 D压强 E刻度线
②将下列操作填写完整,并排列其正确的操作顺序(用字母表示,每个字母只能用一次) ;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡。
B.用量筒准确量取浓盐酸 mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。
C.将已冷却的盐酸沿玻璃杯注入 中。
D.将容量瓶盖紧,颠倒摇匀。
E.改用 加水,使溶液凹液面恰好与刻度相切。
F.继续往容量瓶内小心加水,直到液面接近刻度 处。
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”、“偏小”、“无影响”)。
Ⅰ 用量筒量取浓盐酸时俯视观察凹液面
Ⅱ 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
Ⅲ 定容时仰视刻度线
Ⅳ 溶液注入容量瓶前没有冷却至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色。判断下列说法中不正确的是( )
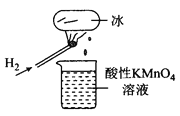
A. 该条件下H2燃烧生成了既具有氧化性又具有还原性的物质
B. 该条件下H2燃烧的产物中可能含有一定量的H2O2
C. 将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性
D. 酸性FeSO4溶液中加入双氧水的离子反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com