
已知反应:2SO2(g)+O2(g) 2SO3(g) 。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)、温度(T)的关系分别如图甲、丙所示。
2SO3(g) 。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)、温度(T)的关系分别如图甲、丙所示。
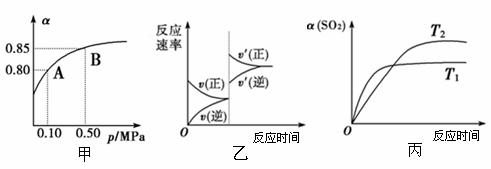
则下列说法正确的是
A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.由图丙知,T1>T2,且该反应的正反应为放热反应
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
已知反应4CO(g)+2NO2(g) N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
A.v(CO)=1.5 mol·L-1·min-1
B.v(NO2)=0.7 mol·L-1·min-1
C.v(N2)=0.4 mol·L-1·min-1
D.v(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
以下现象与电化腐蚀无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 B.生铁比软铁芯(纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处易生铁锈 D.银质奖牌久置后表面变暗
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A.加入适量的6 mol·L-1的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
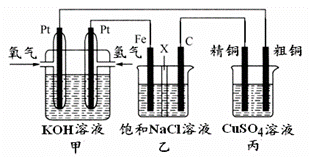
根据要求回答相关问题:
(1)通入氢气的电极为 (填“正极”或“负极”),负极的电极反应式为 。
(2)石墨电极为 (填“阳极”或“阴极”), 乙装置中阳极的电极反应式为_____________。
(3)反应一段时间后,在乙装置中滴入酚酞溶液, _ 区(填“铁极”或“石墨极”)的溶液先变红。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 (填“增大”“减
小”或“不变”)。
(5)若在标准状况下,有224m L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为 ;丙装置中阴极析出铜的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在前一种分散系中慢慢滴加后一种试剂,能观察到先有沉淀生成后变澄清的是
①氯化铝溶液中滴加氢氧化钠溶液
②偏铝酸钠溶液中滴加盐酸
③氢氧化钠溶液中滴加氯化铝溶液
④蛋白质溶液中滴加硫酸铜溶液
⑤氯化铝溶液中滴加氨水
⑥硝酸银溶液中滴加氨水
⑦氢氧化铁胶体中滴加硫酸
A. ①②⑥⑦ B. ②③⑤⑦ C. ①②④⑥ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
A.①③⑤ B.②④ C.①③ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com