
用如图装置实验,下列预期实验现象及相应结论均正确的是
a | b | 预期实验现象 | 结论 |
| |
A | 铜丝 | 浓硝酸 | 试管C中有大量红棕色气体 | 硝酸有强氧化性 | |
B | 木条 | 18.4mol/L 硫酸 | 木条变黑 | 浓硫酸有酸性及氧化性 | |
C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 | |
D | 铁丝 | 含少量HCl的H2O2溶液 | 试管C中有大量无色气体 | 该反应中铁作催化剂 |
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
若醋酸用HAc表示,则在0.1mol·L-1NaAc溶液中,下列离子浓度关系正确的是
A.c(Na+)=c(Ac—)+c(HAc)
B.c(Na+)+c(OH—)=c(Ac—)+c(H+)
C.c(Na+)>c(OH—)>c(Ac—)>c(H+)
D.c(Na+)>c(Ac—)>c(H+)>c(OH—)
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学试卷(解析版) 题型:填空题
【化学——选修物质结构与性质】
X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于 区,单质X的晶体类型为 ,其中X原子的配位数为 。
(2)已知元素Y可与元素Z的相对原子质量只差为16,则元素Y基态原子的外围电子排布图为 ,其同周期元素中,第一电离能最大的是________________(写元素符号)。元素Y的含氧酸中,酸性最强的是_____________(写化学式),该酸根离子的立体构型为_____________。
(3)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(5)X与Y形成的一种化合物的立方晶胞如图所示。
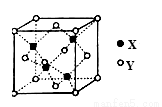
该化合物的化学式为_______________,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是 cm。(写出计算式,不要求计算结果。)
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上月考四化学卷(解析版) 题型:选择题
已知某种微生物燃料电池工作原理如图所示。下列有关该电池的说法中,正确的是

A.外电路电子从B极移向A极[来
B.溶液中H+由B极区移向A极区
C.电池工作一段时间后B极区溶液的pH减小[
D.A极电极反应式为:CH3COOH - 8e-+ 2H2O = 2CO2 + 8H+
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:填空题
工业上可以利用废气中的CO2为原料制取甲醇。请回答下列问题:
(1) 已知常温常压下,下列两个可逆反应的能量变化如下图所示:
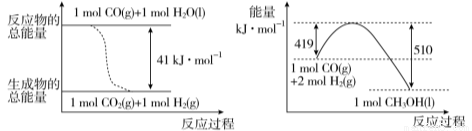
请写出左图反应的平衡常数表达式K= 。
请写出由二氧化碳和氢气制备甲醇的热化学方程式 。
(2) 如果只改变一个条件使上述反应方程式的平衡常数K值变大,则该反应________(选填编号)。
A.一定向正反应方向移动 B.在平衡移动时,正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时,逆反应速率先减小后增大
(3) 在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是________(填字母)。
A.H2的浓度减小 B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加 D.重新平衡时,n(H2)/n(CH3OH)增大
(4) 保持温度和体积不变,通入1molCO2和3molH2 ,下列能说明该反应已达平衡状态的是________(填字母)。
,下列能说明该反应已达平衡状态的是________(填字母)。
A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
B.容器内压强保持不变
C.H2的消耗速率与CO2的消耗速率之比为3∶1
D.容器内气体的平均相对分子质量保持不变
(5) 若反应容器的容积为2.0 L,反应时间4.0 min,容器 内气体的密度减少了2.0 g·L-1。在这段时间内CO2的平均反应速率为_______________
内气体的密度减少了2.0 g·L-1。在这段时间内CO2的平均反应速率为_______________
(6) 有人设计甲醇-空气燃料电池电源, 用石墨作电极电解200 mL含有下列离子的溶液:
用石墨作电极电解200 mL含有下列离子的溶液:
离子 | Cu2+ | H+ | Cl- | SO |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,标况下当两极收集到相同体积的气体时,阳极上收集到氧气的质量为____________(忽略溶液体积的变化及电极产物可能存在的溶解现象)。也有人用此电源利用电解法制备Na2FeO4,阳极材料为铁,其电解质溶液用NaOH溶液,阳极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列说法正确的是
A.H2(g)+Br2(g)=2HBr(g) ΔH=-72 kJ·mol-1其他相关数据如下表:

则表中a为230
B.已知:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1
所以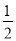 H2SO4(aq)+
H2SO4(aq)+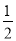 Ba(OH)2(aq)=
Ba(OH)2(aq)=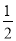 BaSO4(s)+H2O(l)ΔH=-57.3kJ·mol-1
BaSO4(s)+H2O(l)ΔH=-57.3kJ·mol-1
C.已知CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-802.33kJ·mol-1,则CH4的燃烧热为802.33kJ·mol-1
D.已知2C(s)+2O2(g)=2CO2(g)ΔH1 ,2C(s)+O2(g)=2CO(g)ΔH2,则ΔH1>ΔH2
,2C(s)+O2(g)=2CO(g)ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列离子在指定溶液中一定能大量共存的是
A.加入Al能放出H2的溶液中:Fe2+、K+、NO 、Cl-
、Cl-
B.在pH=13的溶液中:Na+、AlO2-、NO 、S2-、SO
、S2-、SO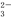
C.由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-、NO 、NH
、NH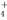 、F-
、F-
D.NaHCO3溶液中:K+、Na+、SO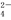 、Al3+
、Al3+
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
红色溶液X中通入气体Y,溶液逐渐褪色,下列对X、Y的推断正确的是( )
A.若X为品红溶液,则Y一定是Cl2或SO2
B.若X为含酚酞的氢氧化钠溶液,则Y可能是SO2
C.若X为含KSCN的氯化铁溶液,则Y一定是HI
D.若X为含硫酸氢钠的石蕊溶液,则Y可能是SO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高二上期中化学卷(解析版) 题型:选择题
下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
A.增大反应物的浓度,活化分子百分数增加,反应速率加快
B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快
C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com