
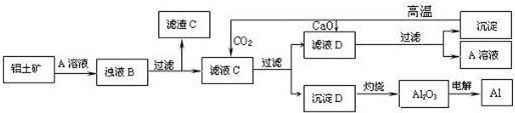
分析 铝土矿的主要成分是Al2O3,此外还含有少量CuO、Fe2O3 等杂质,先用A溶液溶解铝土矿,则A溶液为NaOH溶液,过滤后得到的滤渣C为CuO、Fe2O3;滤液C中溶质为偏铝酸钠;偏铝酸钠溶液中通入二氧化碳气体,反应生成沉淀D氢氧化铝沉淀和滤液D碳酸钠溶液;滤液D中进入氧化钙生成碳酸钙沉淀,过滤后得到碳酸钙沉淀,碳酸钙高温分解生成氧化钙和二氧化碳气体;溶液A中溶质为氢氧化钠;加热沉淀D氢氧化铝分解生成氧化铝,电解氧化铝得到金属铝,
(1)氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,据此写出反应的离子方程式;
(2)CuO、Fe2O3等杂质不与氢氧化钠溶液反应,过滤后得到的滤渣C为CuO、Fe2O3;根据过滤操作方法判断使用的仪器;
(3)根据用铝土矿为原料制备铝的工艺流程及分析判断可以循环使用的物质;
(4)滤液C中含有偏铝酸钠,偏铝酸钠与二氧化碳反应生成氢氧化铝沉淀和碳酸钠;
(5)产生的气体中不含氧气,放出气体平均摩尔质量为36g•mol-1,说明生成的气体是一氧化碳和二氧化碳的混合物,设一氧化碳的物质的量为x、二氧化碳的物质的量为y,根据电子守恒及平均摩尔质量列式计算出二氧化碳和一氧化碳的物质的量,再利用质量守恒定律计算出C的质量.
解答 解:铝土矿的主要成分是Al2O3,此外还含有少量CuO、Fe2O3 等杂质,先用A溶液溶解铝土矿,则A溶液为NaOH溶液,过滤后得到的滤渣C为CuO、Fe2O3;滤液C中溶质为偏铝酸钠;偏铝酸钠溶液中通入二氧化碳气体,反应生成沉淀D氢氧化铝沉淀和滤液D碳酸钠溶液;滤液D中进入氧化钙生成碳酸钙沉淀,过滤后得到碳酸钙沉淀,碳酸钙高温分解生成氧化钙和二氧化碳气体;溶液A中溶质为氢氧化钠;加热沉淀D氢氧化铝分解生成氧化铝,电解氧化铝得到金属铝,
(1)铝土矿中的氧化铝和氢氧化钠反应生成偏铝酸钠和水,反应的离子方程式为:2OH-+Al2O3═2AlO2-+H2O,
故答案为:2OH-+Al2O3═2AlO2-+H2O;
(2)CuO、Fe2O3不和氢氧化钠溶液反应,过滤得到滤渣为CuO、Fe2O3;过滤操作使用的玻璃仪器有:烧杯、漏斗、玻璃棒,
故答案为:CuO、Fe2O3;烧杯、漏斗、玻璃棒;
(3)根据分析可知,可以循环利用的物质有:CaO、H2O、CaCO3、CO2、NaOH,所以除CaO、H2O可以循环使用外,还可以循环使用的物质有:CaCO3、CO2、NaOH,
故答案为:CaCO3、CO2、NaOH;
(4)滤液C中含有偏铝酸钠,偏铝酸钠与二氧化碳反应的离子方程式为:CO2+AlO2-+2 H2O=Al(OH)3↓+HCO3-,
故答案为:CO2+AlO2-+2 H2O=Al(OH)3↓+HCO3-;
(5)54t铝的物质的量为:$\frac{54×1{0}^{6}}{27g/mol}$=2×106mol,
产生的气体中不含氧气,放出气体平均摩尔质量为36g•mol-1,说明生成的气体是一氧化碳和二氧化碳的混合物,根据电子守恒可知,从氧化铝得到金属铝得到的电子与阳极C与氧气反应生成一氧化碳、二氧化碳时转移电子数相同,
设一氧化碳的物质的量为x、二氧化碳的物质的量为y,则根据电子守恒可得:①2x+4y=2×106mol×3,根据气体平均摩尔质量可得:②$\frac{28x+44y}{x+y}$=36,根据①②可得:x=y=106mol,根据C原子守恒,阳极消耗的C的质量为:12g/mol×(106mol+106mol)=24×106g=24t,
故答案为:24.
点评 本题考查了铝及其化合物的性质,题目难度中等,涉及化学实验基本操作方法的应用、离子方程式的书写、化学计算、铝及其化合物性质等知识,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验、化学计算能力.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2作氧化剂,发生还原反应 | |
| B. | 钾元素化合价降低 | |
| C. | 该反应是置换反应 | |
| D. | 每生成2 mol K2FeO4,转移3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
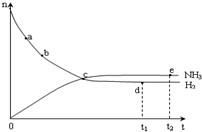 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A. | 点a的正反应速率比点b的大 | |
| B. | 点c处反应达到平衡 | |
| C. | 点d(t1时刻) 和点e(t2时刻)处n(N2)不一样 | |
| D. | 点d正反应速率和点 e的逆反应速率一样 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.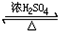 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
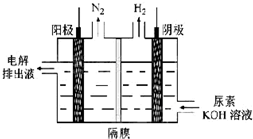 碳及其化合物的研究具有重要的现实意义
碳及其化合物的研究具有重要的现实意义| 物质 T/℃n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
 N2+CO2.
N2+CO2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
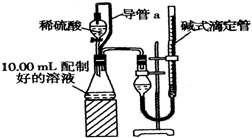 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高分子分离膜应用于食品工业中,可用来浓缩天然果汁、乳制品加工、酿造业等 | |
| B. | 复合材料一般是以一种材料做基体,另一种材料作为增强剂 | |
| C. | 合成高分子材料制成的人工器官一般都受到人体的排斥,难以达到生物相容的程度 | |
| D. | 导电塑料是应用于电子工业的一种新型有机高分子材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com