
| 结构简式 | 系统命名法命名 | |
| 可能1 | ||
| 可能2 | ||
| … |
| V |
| Vm |
| m |
| n |
| △ |
| △ |
| H2O |
| △ |
| H2O |
| △ |
| V |
| Vm |
| 4.48L |
| 22.4L/mol |
| m |
| n |
| 11.6g |
| 0.2mol |
| mVm |
| V |
| 11.6g×22.4mol/L |
| 4.48L |
| 点燃 |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
| 检测次数 | 溶液中检测出的溶质 |
| 第一次 | KCl、K2SO4、Na2CO4 |
| 第二次 | BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3 |
| 实验步骤 | 实验操作 | 实验目的 | 离子反应 |
| 第一步 | 向溶液中滴加过量的HNO3溶液 | 检验 |
|
| 第二步 | 继续滴加过量的Ba(NO3)2溶液 | 检验SO42-的存在 | |
| 第三步 | 过滤,再向滤液中滴加 |
检验 |
Ag++Cl-=AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 | 48h后 |
| pH | 5.0 | 4.8 | 4.6 | 4.3 | 4.2 | 4.0 | 4.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
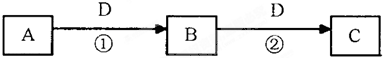
 有关短周期元素A、B、C、D、E、F的信息如下:
有关短周期元素A、B、C、D、E、F的信息如下:| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | 其单质是淡黄色固体 |
| F | 最高正价与最低负价代数和为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
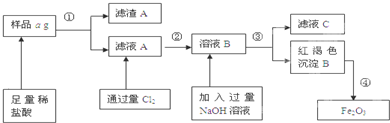
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
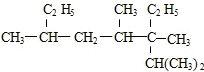
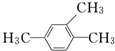
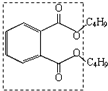 含有的官能团名称为
含有的官能团名称为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com