
| A.(b-a)/3mL | B.(a-b)/3mL |
| C.(4b-1)/13mL | D.3/(b-a)mL |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.20mL | B.25mL | C.28mL | D.33mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
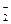 +xI-+yH+=bNO↑+cI2+zH2O,
+xI-+yH+=bNO↑+cI2+zH2O,查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2与H2在一定条件下反应生成NH3 | B.NO与O2反应生成NO2 |
| C.由NH3制NH4HCO3和(NH4)2SO4 | D.NH3经催化氧化生成NO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.火箭点火后瞬间,逸出红棕色气体是NO2 |
| B.偏二甲基肼[(CH3)2—N—NH2]与均二甲基肼[CH3NH—NH—CH3]沸点不相同 |
| C.每生成3 mol氮气,转移电子的物质的量为16 mol |
| D.在宇宙飞船船舱中比在地球上更容易做过滤实验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若金属有剩余,则剩余金属一定含Cu . |
B.若硝酸溶液体积为100ml,反应后金属有剩余,则可计算产 生NO的物质的量. 生NO的物质的量. |
| C.若金属恰好全部溶解后,再加硝酸溶液仍能产生NO. |
| D.若金属全部溶解,则溶液中一定含Fe3+、Cu2+. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
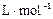 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com