
【题目】回答下列各题:
(1)相同质量的O2和O3所含氧原子的个数比为______,标准状况下气体的体积之比为_______;
某19g二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是_______。
(2)某反应中反应物与生成物有:NH3、H2SO4、KClO3、K2SO4、HNO3、H2O和一种未知物质X。
①已知 KClO3在反应中得到电子,则该反应的还原剂是____。
②已知 0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为____。
③根据上述反应可推知还原性: NH3____X (填>、<符号)。
(3)已知反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑ ⑤Na2O+H2O=2NaOH ⑥Fe2O3+3H2![]() 2Fe+3H2O
2Fe+3H2O
上述反应中,不属于氧化还原反应的有_________(填序号,下同);H2O只做氧化剂的是_____;属于氧化还原反应,但反应物中的H2O既不被氧化也不被还原的是________。
(4)反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O能制备氯气,该反应中,氧化剂是______________。反应中被氧化的HCl和未被氧化HCl的物质的量之比为________。
(5)铜与稀硫酸、双氧水混合能制备硫酸铜,写出反应的离子方程式:_______________________。
【答案】1:1 3:2 95g/mol NH3 Cl2 > ①⑤ ④ ② KMnO4 5:3 Cu+2H++H2O2=Cu2++2H2O
【解析】
(1)先根据氯化物的分子式ACl2,由Cl-的物质的量求出氯化物的物质的量,再根据公式M=![]() 来确定分子的摩尔质量;
来确定分子的摩尔质量;
(2)KClO3在反应中得到电子,所以KClO3是氧化剂,发生还原反应,被还原,NH3变成了HNO3,所以NH3是还原剂;
(3)含元素化合价变化的反应为氧化还原反应,水被氧化,则水中O元素的化合价升高,水被还原,则水中H元素的化合价降低;若水中H、O元素的化合价不变,则H2O既不被氧化,又不被还原;
(4)反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中Mn元素化合价由+7价降低到+2价,被还原,KMnO4为氧化剂;
(5)铜与稀硫酸、双氧水混合反应生成硫酸铜和水。
(1)设其质量为m,等质量的O2和O3所含分子个数比=![]() =3:2,一个氧气分子中含有2个氧原子,一个臭氧分子中含有3个氧原子,所以其氧原子个数=(3×2):(2×3)=1:1;
=3:2,一个氧气分子中含有2个氧原子,一个臭氧分子中含有3个氧原子,所以其氧原子个数=(3×2):(2×3)=1:1;
标准状况下气体的体积之比为![]() =3:2;
=3:2;
因氯化物ACl2中含有0.4molCl-可知,氯化物ACl2的物质的量为![]() =0.2mol,则M(ACl2)=
=0.2mol,则M(ACl2)=![]() =95g/mol;
=95g/mol;
(2)①KClO3在反应中得到电子,所以KClO3是氧化剂,发生还原反应,被还原,NH3变成了HNO3,所以NH3是还原剂,故答案为:NH3;
②设X中氯元素的化合价为x,则0.2mol(5-x)=1mol,所以x=0,故X为Cl2,故答案为:Cl2;
③在反应中,氧化剂为KClO3,还原剂为NH3,氧化产物为HNO3,还原产物为Cl2,由氧化剂的氧化性大于氧化产物的氧化性可知KClO3> HNO3,由还原剂的还原性大于还原产物的还原性可知NH3>X (Cl2);
(3)只有①⑤反应中没有元素的化合价变化,不属于氧化还原反应;
只有④水中O元素的化合价升高,水被还原,水作氧化剂;
只有②中属于氧化还原反应,但水中H、O元素的化合价不变,则H2O既不被氧化,又不被还原;
(4)反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中Mn元素化合价由+7价降低到+2价,被还原,KMnO4为氧化剂;
反应中16molHCl参加反应,其中10mol被氧化,另外6mol作为酸与金属离子结合,则被氧化与未被氧化的HCl的质量之比比为5:3;
(5)铜与稀硫酸、双氧水混合反应生成硫酸铜和水,反应的离子方程式为Cu+2H++H2O2=Cu2++2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42-、CO32-、I-、Cl-中的一种或多种,进行如图所示的实验,下列说法正确的是 ( )
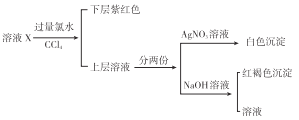
A. 溶液X中有Fe3+、SO42-
B. 溶液X中有Fe2+、I-可能有SO42-、Cl-
C. 溶液X中有I-、Cl-,无CO32-
D. 溶液X中有I-,Fe2+和Fe3+两种离子中至少有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,已知醋酸的电离常数Ka=1.6×10-5,醋酸银的溶度积Ksp(CH3COOAg)=3.7×10-3。下列有关说法正确的是
A. 醋酸溶液中,c(CH3COO-)>c(H+)>c(OH-)
B. 将相同浓度的CH3COOH溶液与CH3COO Na溶液等体积混合,所得溶液呈碱性
C. 该温度下,1mol/L的醋酸溶液中,醋酸的电离度为0.4%
D. 该温度下,浓度均为0.02mol/L的CH3COONa溶液和AgNO3溶液等体积混合(忽略混合后溶液体积的变化),有CH3COOAg沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 将H2O2滴加到酸性KMnO4溶液中:2MnO4-+ H2O2 + 6H+ === 2Mn2+ + 3O2↑+ 4H2O
B. 在NH4HSO4溶液中慢慢滴入等物质的量的NaOH溶液:NH4++ OH- === NH3·H2O
C. 用惰性电极电解氯化钠溶液:2H+ + 2Cl- === H2↑ + Cl2↑
D. 用酸性高锰酸钾溶液滴定草酸:2MnO4-+ 5H2C2O4 + 6H+ === 2Mn2+ + 10CO2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种碳骨架如下的烃。下列说法正确的是( )
![]()
①a和d是同分异构体 ②b和c是同系物 ③a和d都能发生加聚反应 ④只有b和c能发生取代反应
A. ①② B. ①④
C. ②③ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好。该佛像未锈蚀的主要原因是()
A. 铝不易发生化学反应 B. 铝的氧化物容易发生还原反应
C. 铝不易被氧化 D. 铝易氧化,但氧化铝具有保护内部铝的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.可溶性铜盐有毒,生命体中不含铜元素
B.金属材料分为黑色金属材料和有色金属材料
C.光线通过胶体时,看到的光柱是被胶体粒子散射的现象
D.稀土金属用途广泛被誉为 新材料的宝库,可单独使用,亦可用于生成合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L1硫酸、6 mol·L1盐酸和蒸馏水)

回答下列问题:
(1)装置A中发生反应的化学方程式是______________________________________。
(2)装置B的作用是______________,装置C的作用是______________,装置E的作用是_____________。
(3)装置D中发生反应的化学方程式是______________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1molL—1二元弱酸H2A溶液的pH,溶液中的H2A、HA—、A2—的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=c(x)/[c(H2A)+c(HA—)+c(A2—)]。下列叙述错误的是
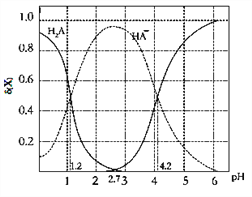
A. 向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离程度一直增大
B. K2(H2A)=10﹣4.2
C. pH=2.7时,[c(HA—)]2/[c(H2A)c(A2—)]=100
D. pH=4.2时,c(HA﹣) =c (A2—)且c(H2A)≈0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com