
已知反应:① 101kPa时,C(s) + 1/2O2(g)=CO(g);△H1=-110.5kJ/mol
② 稀溶液中,H+(aq) + OH-(aq)=H2O(1);△H2=-57.3kJ/mol
下列结论正确的是 ( )
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.浓硫酸与稀NaOH溶液反应的中和热值为57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
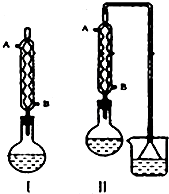 由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:
由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:| 浓H2SO4 |
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在以上条件下,向体积不变的密闭容器中通入1 mol SO2和0.5 mol O2,反应达到平衡时放出热量为Q1 kJ;在同样的条件下向同样的密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量为Q2 kJ。则下列关系正确的是( )
A.2Q1=Q2 B.2Q1>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101 kPa时,2C(s)+O2(g)====2CO(g);ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-====(aq)H2O(l);ΔH=-57.3 kJ·mol-1
下列结论正确的是 ( )
A.碳的燃烧热大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com