
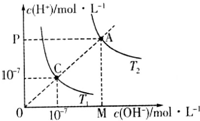
| A、水的离子积常数关系为:C>A |
| B、升高温度可实现由C点到A点 |
| C、T1时,pH=4的硫酸与pH=l0的氢氧化钠溶液等体积混合,所得溶液的pH=7 |
| D、图中矩形OMAP的面积表示T2时水的离子积的值 |


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
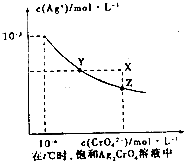 ①已知t℃时AgCl的Kap为2×10-10;②在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
①已知t℃时AgCl的Kap为2×10-10;②在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A、在t℃时,反应Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107 |
| B、在t℃时,Ag2CrO4的Kap为1×10-9 |
| C、在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| D、在t℃时,以0.01molL-1AgNO3溶液滴定20mL O.01molL-1KC1和0.01molL-1的K2CrO4的混和溶液,CrO42-先沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 稀盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 硫酸钡 | 一水合氨 | 二氧化硫 |
| C | 胆矾 | 稀硫酸 | 铁 | 水 | 碳酸钙 |
| D | 明矾 | 氢氧化铁胶体 | 氯化钠 | 次氯酸 | 氯气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=7的NH4Cl与氨水的混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
| B、0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| D、常温下,pH=2的CH3COOH与pH=12的NaOH等体积混合:c (CH3COO-)+c(H+)>c(Na+)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从合成塔出来的气体,其中氨气一般占15%,所以生产氨的工业的效率都很低 |
| B、由于NH3易液化,N2、H2可循环使用,则总的说来氨的产率很高 |
| C、合成氨工业的反应温度控制在400~500℃左右,是因为该条件下氨的产率最高 |
| D、合成氨工业采用10 MPa~30MPa,是因该条件下催化剂的活性最好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
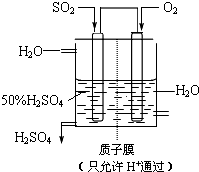 某人设想以如图所示装置用电化学原理生产硫酸,写入通入SO2的电极的电极反应式
某人设想以如图所示装置用电化学原理生产硫酸,写入通入SO2的电极的电极反应式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

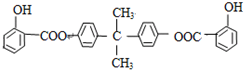
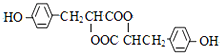
查看答案和解析>>
科目:高中化学 来源: 题型:
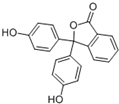
| A、分子式为C20H14O4 |
| B、可以发生取代反应、加成反应、氧化反应 |
| C、含有的官能团有羟基、酯基 |
| D、1mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10mol和4mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com