
室温下,将盐酸和氨水等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/mol·L-1 | 反应后溶液的pH | |
| c(氨水) | c(HCl) | ||
| ① | 0.1 | 0.1 | 5 |
| ② | 0.2 | x | 7 |
下列叙述错误的是( )
A.实验②反应后的溶液中:c(NH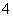 )+c(NH3·H2O)>0.1 mol·L-1
)+c(NH3·H2O)>0.1 mol·L-1
B.实验①反应后的溶液中c(H+)=c(Cl-)+c(OH-)-c(NH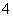 )
)
C.实验①反应后的溶液中:c(Cl-)>c(NH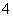 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.实验②反应后的溶液中:c(NH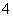 )=c(Cl-)>c(OH-)=c(H+)
)=c(Cl-)>c(OH-)=c(H+)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
利用提供的试剂(硫酸铜、氯化钠、硫酸、乙醇、橙汁、NaOH溶液)和材料(石墨、锌片、铜片、塑料、导线),完成对Zn+Cu2+ Zn2++Cu的原电池设计。
Zn2++Cu的原电池设计。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种方法中,能对金属起到防止或减缓腐蚀作用的是( )
①金属表面涂抹油漆 ②改变金属内部结构 ③保持金属表面清洁干燥 ④金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜
A.①②③④ B.①③④⑤ C.①②④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片作负极,铜片作正极,在CuSO4溶液中,铜片质量增加
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出的速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
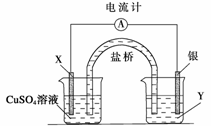
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的__________极,发生的电极反应为______________________;
X电极上发生的电极反应为_______________________________________________;
(3)外电路中的电子是从__________电极流向__________电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表所示:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是( )
A.2CN-+H2O+CO2===2HCN+CO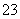
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C.物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-)
D.c(NH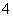 )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述的实验能达到预期目的的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 滴定实验中,用待测液润洗锥形瓶2~3次 | 避免造成实验误差 |
| B | 向氯水中滴加AgNO3、稀HNO3溶液,产生白色沉淀 | 验证氯水中含有Cl- |
| C | 向盛有沸水的烧杯中滴加饱和氯化铁溶液并长时间煮沸 | 制备氢氧化铁胶体 |
| D | 向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1 mol·L-1 MgCl2溶液,再加入3滴1 mol·L-1 FeCl3溶液 | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为某有机物的结构简式。已知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下: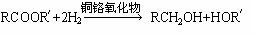
关于该化合物的下列说法中,不正确的是( )
A、该有机物的化学式为C20H14O5
B、该有机物可以与浓溴水反应
C、与足量氢氧化钠溶液充分反应,所得产物中有醇类物质
D、1mol该有机物在铜铬氧化物催化下仅能与2mol氢气发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com