
���� ��1���ٸ�������к͵ζ����������������
�ڸ�������������������ȫ��Ӧ����Һ�����ԣ���ѡ���̪����ȣ�
�۸��ݵζ�����ǰ������Һ����ɫ����Ӧ��������Һ����ɫ�仯�жϵζ��յ㣻
��2����ʽ�ζ���������ˮ��ϴ��δ�ñ�Һ��ϴ��������������Һ��Ũ�ȱ�С��
�۲��ʽ�ζ��ܶ���ʱ�����ζ�ǰ���ӣ������ƫ�ζ����ӣ������ƫС��
��3���ȸ��ݵζ����ĵ�����������Һ���������Ӧ����ʽ���������Һ��������ʵ���Ũ�ȣ��ٸ���ϡ��ǰ�����ʵ����ʵ������������㣮
��� �⣺��1�����ñ�0.14mol/L NaOH��Һ�ζ������ʵ���������Ϊ�����ζ����Ƿ�©ˮ��ϴ�ӵζ��ܡ���ϴ��ʢװ��Һ����ϴʢװ��Һ�ĵζ��ܡ�ʢװ��Һ����ʼ�ζ����ظ��ζ��ȣ�������ȷ�IJ���˳��Ϊ��ECDBAGF����ECBADGF����
�ʴ�Ϊ��ECDBAGF����ECBADGF����
������������������ȫ��Ӧ����Һ�����ԣ���ѡ���̪����ȣ�
�ʴ�Ϊ����̪����ȣ�
����ѡ���̪���۲쵽��ƿ����Һ����ɫ��dz��ɫ��Ϊ��ɫ���ﵽ�ζ��յ㣻��ѡ����ȣ��۲쵽��Һ�ɻ�ɫ��Ϊ��ɫ����ﵽ�ζ��յ㣻
�ʴ�Ϊ����̪Ϊָʾ��ʱdz��ɫ��Ϊ��ɫ�Ұ���Ӳ���ԭ�������Ϊָʾ��ʱ��ɫ��ɫ��ɫ�Ұ���Ӳ���ԭ����
��2����ʽ�ζ���������ˮ��ϴ��δ�ñ�Һ��ϴ���൱�ڱ�Һ��ϡ�ͣ��������ĵ���ϡ����ͻ����࣬�ζ����ƫ��
�ʴ�Ϊ��ƫ��
��ʽ�ζ��ܵζ�ǰ����ʱ���ӣ������ƫ����ʱ����ƽ�ӣ���������䣬����������Ƿ�Ӧ���ĵ��������Ƶ����������������ƫС�������ĵ��������Ƶ����ƫС�������������ʵ���Ũ��ƫС��
�ʴ�Ϊ��ƫС��
��3����0.14mol/L��NaOH��Һ�ζ�����ϡH2SO4 25mL���ζ���ֹʱ����NaOH��Һ15mL�����ݷ�Ӧ��2NaOH+H2SO4=Na2SO4+2H2O��ϡ�ͺ��������ҺŨ��c��H2SO4��=$\frac{\frac{1}{2}��0.14mol/L��0.015L}{0.025L}$=0.042mol/L���������ᣨϡ��ǰ�����ᣩ��Һ�����ʵ���Ũ��c��H2SO4��=$\frac{0.042mol/L��100mL}{1.00mL}$=4.2mol/L��
�ʴ�Ϊ��4.2��
���� ���⿼��������к͵ζ�ʵ����������������������к͵ζ���ʵ�鲽���ע��������ؿ���ѧ������������ʵ����������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
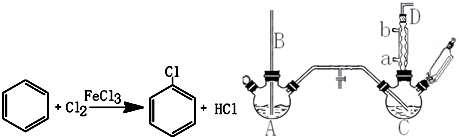
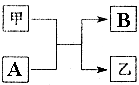 ����A��B�뻯����ס�������ͼ��ʾ��ת����ϵ����Ҫ�ķ�Ӧ����δ��������ش��������⣺
����A��B�뻯����ס�������ͼ��ʾ��ת����ϵ����Ҫ�ķ�Ӧ����δ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
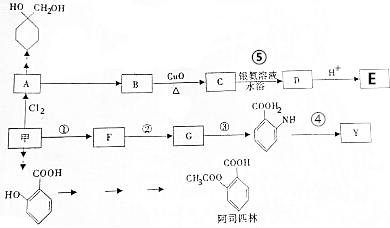
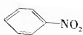 $\stackrel{Fe/HCl}{��}$
$\stackrel{Fe/HCl}{��}$ ���������ױ���������
���������ױ��������� �������13��ԭ�ӹ��森
�������13��ԭ�ӹ��森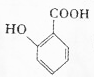 ������Ϊ���ǻ������ᣬG�й���������Ϊ�Ȼ���������
������Ϊ���ǻ������ᣬG�й���������Ϊ�Ȼ��������� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ŀ | ���ȱ� | β�� | ��ȷ������ | ��ʧ���� |
| ����ʧ����kg/t�� | 13 | 24.9 | 51.3 | 89.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
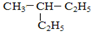 ��
��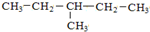
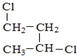 ��
�� ��H2O��D2O
��H2O��D2O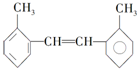 �䱽���ϵ�һ�ȴ�����4�֣�1mol�����ʺ���ˮ��ϣ�����Br2�����ʵ���Ϊ1mol��
�䱽���ϵ�һ�ȴ�����4�֣�1mol�����ʺ���ˮ��ϣ�����Br2�����ʵ���Ϊ1mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6 | B�� | 7 | C�� | 8 | D�� | 9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
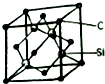 ͭ���ء��������Ԫ�صĻ�����������������̫���ܵ�ص���Ҫ���ϣ���ش�
ͭ���ء��������Ԫ�صĻ�����������������̫���ܵ�ص���Ҫ���ϣ���ش�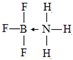 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com