
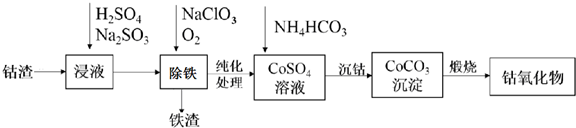
���� ����[��Co��OH��3��Fe��OH��3��]��������������ƽ�Һ��Co��OH��3��Fe��OH��3�ܽ⣬2Co��OH��3+4H++SO32-=2Co2++SO42-+5H2O��Fe��OH��3�������ܽ��Ϊ�����ӣ������������Ʒ���������ԭ��Ӧ�����������ӣ��ڽ�Һ��ͨ�����������������Ƴ�������������������̼����泥��õ�CoCO3���������պ�õ��ܵ������
��1���ڽ�Һ��ͨ������������������ʱ�������ӱ�����Ϊ�����ӣ����ܹ�����CoSO4��NH4HCO3��Ӧ����CoCO3����������李�������̼��ˮ������ԭ���غ���д��ѧ����ʽ��
��2������̼ԭ���غ㣬n��CO2��=n��CoCO3�����ٸ���V=nVm����CoCO3��������������õ�CO2�������
��3���ɵ����غ㣺n��Co3+��=2 n��Cl2�����ɵ���غ㣺n��Coԭ�ӣ���=n��Co2+����Һ=$\frac{1}{2}$n��Cl-������������n��������Co2+�������ݻ��ϼ۵���غ�Ϊ0������������n��O��������������������n��Co����n��O����
��� �⣺��1�����Ʊ����̿�֪���������ܽ��Ϊ�����ӣ������������Ʒ���������ԭ��Ӧ�����������ӣ��ڽ�Һ��ͨ������������������ʱ�������ӱ�����Ϊ�����ӣ���֪��������Ԫ�صĻ��ϼ�Ϊ+3�ۣ����ܹ�����CoSO4��NH4HCO3��Ӧ���õ�CoCO3����������ԭ���غ㣬�÷�Ӧ�Ļ�ѧ����ʽΪ��CoSO4+2NH4HCO3=CoCO3��+��NH4��2SO4+CO2��+H2O��
�ʴ�Ϊ��+3��CoSO4+2NH4HCO3=CoCO3��+��NH4��2SO4+CO2��+H2O��
��2��119g CoCO3���������ʵ���Ϊn��CoCO3��=$\frac{m}{M}$=$\frac{119g}{119g/mol}$=1mol��CoCO3����������գ��������������CO2������̼ԭ���غ㣬n��CO2��=n��CoCO3����n��CO2��=1mol����״���£�V=nVm=1mol��22.4L/mol=22.4L��
�ʴ�Ϊ��22.4L��
��3���ɵ����غ㣺n��Co3+��=2n��Cl2��=0.3mol���ɵ���غ㣺n��Co����=n��Co2+����Һ=$\frac{1}{2}$n��Cl-��=0.5����1.5mol-0.15mol��2��=0.6mol��
���Թ����е�n��Co2+��=0.6mol-0.3mol=0.3mol��n��O��=��0.3mol��3+0.3mol��2����2=0.75mol��
��n��Co����n��O��=0.6mol��0.75mol=4��5��
�ʴ�Ϊ��4��5��
���� ���⿼�������Ʊ�����Ӧ����ʽ����д���й����ʵ����ļ���ȣ����������Ϣ������ܼ��仯���������Ϊ���Ĺؼ�����3���м���ע���غ�˼���Ӧ�ã���Ŀ�Ѷ��еȣ�


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ⱥ��ʳ��ˮ���ռ�������ӽ���Ĥ�����ɷ�ֹ����������Cl2���������� | |
| B�� | ��ˮ����һ���Լ������������ױ����������������� | |
| C�� | ��������������ƣ�����ͼ��ʾװ�� ��ע��bΪ�����ӽ���Ĥ��cΪ�����ӽ���Ĥ�� ��ע��bΪ�����ӽ���Ĥ��cΪ�����ӽ���Ĥ�� | |
| D�� | ��ȩ�����������Թ������10%��NaOH��Һ2 mL������2%��CuSO4��Һ4�Ρ�6�Σ��������ȩ��Һ0.5 mL������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
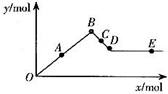 ��֪Ba��AlO2��2������ˮ����ͼ��ʾ������Al2��SO4��3��Һ����μ���Ba��OH��2��Һʱ�����ɳ��������ʵ���y�����Ba��OH��2�����ʵ���x�Ĺ�ϵ�������й�������ȷ���ǣ�������
��֪Ba��AlO2��2������ˮ����ͼ��ʾ������Al2��SO4��3��Һ����μ���Ba��OH��2��Һʱ�����ɳ��������ʵ���y�����Ba��OH��2�����ʵ���x�Ĺ�ϵ�������й�������ȷ���ǣ�������| A�� | A��Dʱ���������ʵ�����Al��OH��3��BaSO4�� | |
| B�� | C��Dʱ��Һ�����ӵ����ʵ�����AlO2-��Ba2+�� | |
| C�� | A��Dʱ���������ʵ�����BaSO4����С��Al��OH��3 | |
| D�� | D��Eʱ��Һ�����ӵ����ʵ�����Ba2+���ܵ���OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �˴Ź����� | B�� | ������� | C�� | ���� | D�� | ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com