
 图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.当电池工作时,下列有关说法正确的是( )
图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.当电池工作时,下列有关说法正确的是( )| A、电池的能量转化率可达100% |
| B、铝罐是电池的负极 |
| C、碳棒应与玩具电机的负极相连 |
| D、电池工作一段时间后碳棒和炭粒的质量会减轻 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
A、当x≤
| ||
| B、当x≥n时,反应的离子方程式为:2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- | ||
| C、当Fe2+和I-都被氧化时,x与n的关系为x>n | ||
| D、当x=n时,反应后氧化产物的物质的量为n mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(A2-)+c(OH-)=c(H2A)+c(H+) |
| B、c(HA-)>c(A2-)>c(H2A) |
| C、c(HA-)>c(H+)>c(OH-) |
| D、c(HA-)>c(OH-)>c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | 溶解度AgCl比AgI大 |
| C | 电石与饱和食盐水制得的气体直接通入溴水 | 溴水褪色 | 乙炔一定发生加成反应 |
| D | 无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
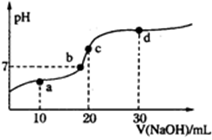 常温时向20mL 0.1mol?L-1 HA溶液中不断滴入0.1mol?L-1 NaOH溶液,pH变化如图.下列叙述正确的是( )
常温时向20mL 0.1mol?L-1 HA溶液中不断滴入0.1mol?L-1 NaOH溶液,pH变化如图.下列叙述正确的是( )| A、HA的电离方程式:HA═H++A- |
| B、水的电离程度:a点>b点 |
| C、c点溶液:c(H+)+c(Na+)═c(A-)+c(HA) |
| D、d点溶液:c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N5+常温下会剧烈爆炸,体积急剧膨胀,放出大量的热 |
| B、N60的发现开辟了能源世界的新天地,将来可能成为很好的火箭燃料 |
| C、N2、N3、N5、N5+、N60互为同素异形体 |
| D、含N5+的化合物中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com