
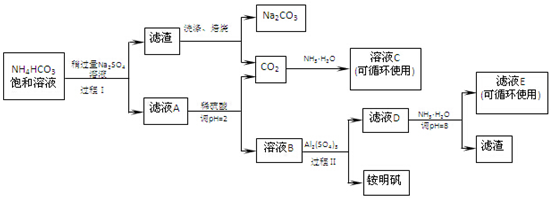
分析 A溶液显碱性,可促进水的电离;D溶液显酸性,A、D溶液焰色反应均为黄色,结合A$?_{E}^{D}$B$?_{E}^{D}$C可知,
(1)若A、B、C中含有相同的金属元素,且B能溶于酸也能溶于碱,A为NaAlO2,B为Al(OH)3,C为Al2(SO4)3,E为NaOH,D能与Ba(OH)2反应生成不溶于盐酸的白色沉淀,且D溶液显酸性,则D为NaHSO4;
(2)若C是一种无色无味的气体,且能使澄清石灰水变浑浊,A为Na2CO3,B为NaHCO3,C为CO2,E为NaOH,以此来解答.
解答 解:A溶液显碱性,可促进水的电离;D溶液显酸性,A、D溶液焰色反应均为黄色,结合A$?_{E}^{D}$B$?_{E}^{D}$C可知,
(1)若A、B、C中含有相同的金属元素,且B能溶于酸也能溶于碱,A为NaAlO2,B为Al(OH)3,C为Al2(SO4)3,E为NaOH,D能与Ba(OH)2反应生成不溶于盐酸的白色沉淀,且D溶液显酸性,则D为NaHSO4,A、C反应生成B的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:NaAlO2;NaHSO4;Al3++3AlO2-+6H2O=4Al(OH)3↓;
(2)若C是一种无色无味的气体,且能使澄清石灰水变浑浊,A为Na2CO3,B为NaHCO3,C为CO2,E为NaOH,A溶液显碱性的原因为CO32-+H2O?HCO3-+OH-;C与E反应生成B的化学方程式为CO2+NaOH=NaHCO3,
故答案为:CO32-+H2O?HCO3-+OH-;CO2+NaOH=NaHCO3.
点评 本题考查无机物的推断,为高频考点,把握钠及Al的化合物之间的相互转化为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:实验题
| 实验序号 | 金属 质量/g | 金属状态 | C(H2SO4) /mol•L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 数据模糊A |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 35 | 数据模糊B |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 数据模糊C |
| 7 | 0.10 | 丝 | 1.0 | 50 | 数据模糊D | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 未测数据 | 40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放出Y kJ | B. | 放出(5X-0.5Y) kJ | C. | 放出(10X-Y) kJ | D. | 吸收(10X-Y) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中醋酸根浓度与醋酸分了浓度比值变大 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 溶液的导电能力增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据要求回答问题:
根据要求回答问题: .
. .分子中可能处于同一平面上的碳原子最多有4个.
.分子中可能处于同一平面上的碳原子最多有4个.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
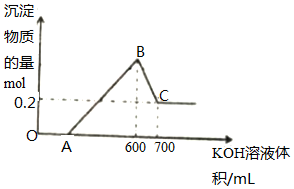 将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体.向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:
将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体.向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 提取碘水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度比水中大 |
| B | 除去纯碱中的碳酸氢铵 | 加热 | 纯碱的热稳定性大于碳酸氢铵 |
| C | 分离KNO3和NaCl | 重结晶 | 硝酸钾的溶解度大于氯化钠 |
| D | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯密度大于乙醇 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com