
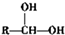 $\stackrel{×Ō¶ÆĶŃĖ®}{”ś}$
$\stackrel{×Ō¶ÆĶŃĖ®}{”ś}$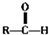 £ØRĪŖōĒ»ł£©
£ØRĪŖōĒ»ł£© £®
£® £®
£®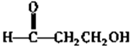 £®
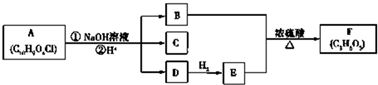
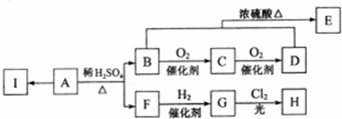
£® ·ÖĪö ÓÉBÓėEŌŚÅØĮņĖį¼ÓČČĢõ¼žĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉF£¬ÓÖBÓėEµÄĻą¶Ō·Ö×ÓÖŹĮæĻąµČ£¬ŌņBĪŖHCOOH£¬EĪŖCH3CH2OH£¬FĪŖHCOOCH2CH3£»DÓėĒāĘų¼Ó³ÉÉś³ÉE£¬ŌņDĪŖCH3CHO£¬AŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ·¢ÉśĖ®½āŌŚĖį»ÆµĆµ½B”¢C”¢D£¬ÓÖCÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬Ōņŗ¬ÓŠ·ÓōĒ»ł£¬ÓÖC±½»·ÉĻµÄŅ»ĀČ“śĪļÓŠĮ½ÖÖ£¬ĖłŅŌĪŖ¶Ō³Ę½į¹¹£¬ŌņCĪŖ £¬AĪŖ
£¬AĪŖ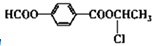 £¬¾Ż“Ė·ÖĪö½ā“š£®
£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗÓÉBÓėEŌŚÅØĮņĖį¼ÓČČĢõ¼žĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉF£¬ÓÖBÓėEµÄĻą¶Ō·Ö×ÓÖŹĮæĻąµČ£¬ŌņBĪŖHCOOH£¬EĪŖCH3CH2OH£¬FĪŖHCOOCH2CH3£»DÓėĒāĘų¼Ó³ÉÉś³ÉE£¬ŌņDĪŖCH3CHO£¬AŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ·¢ÉśĖ®½āŌŚĖį»ÆµĆµ½B”¢C”¢D£¬ÓÖCÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬Ōņŗ¬ÓŠ·ÓōĒ»ł£¬ÓÖC±½»·ÉĻµÄŅ»ĀČ“śĪļÓŠĮ½ÖÖ£¬ĖłŅŌĪŖ¶Ō³Ę½į¹¹£¬ŌņCĪŖ £¬AĪŖ
£¬AĪŖ £¬
£¬
£Ø1£©øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOH£»CĪŖ £¬¹Ź“š°øĪŖ£ŗHCOOH£»
£¬¹Ź“š°øĪŖ£ŗHCOOH£» £»
£»
£Ø2£©øł¾ŻŅŌÉĻ·ÖĪö£¬AĪŖ £¬¹ŁÄÜĶŵÄĆū³ĘŹĒõ„»łŗĶĀČŌ×Ó£»ÓÉÓŚAÖŠŗ¬ÓŠ1øö·Óõ„£¬1øö“¼õ„ŗĶ1øöĀČŌ×Ó£¬1øö·Óõ„ĻūŗÄ2øöNaOH£¬ĖłŅŌ1molA ŌŚ×ćĮæNaOHČÜŅŗÖŠ³ä·Ö·“Ó¦£¬×ī¶ąĻūŗÄNaOHµÄĪļÖŹµÄĮæĪŖ4mol£¬¹Ź“š°øĪŖ£ŗõ„»łŗĶĀČŌ×Ó£»4£»
£¬¹ŁÄÜĶŵÄĆū³ĘŹĒõ„»łŗĶĀČŌ×Ó£»ÓÉÓŚAÖŠŗ¬ÓŠ1øö·Óõ„£¬1øö“¼õ„ŗĶ1øöĀČŌ×Ó£¬1øö·Óõ„ĻūŗÄ2øöNaOH£¬ĖłŅŌ1molA ŌŚ×ćĮæNaOHČÜŅŗÖŠ³ä·Ö·“Ó¦£¬×ī¶ąĻūŗÄNaOHµÄĪļÖŹµÄĮæĪŖ4mol£¬¹Ź“š°øĪŖ£ŗõ„»łŗĶĀČŌ×Ó£»4£»
£Ø3£©øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOH”¢DĪŖCH3CHO£¬
a”¢øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOH”¢DĪŖCH3CHO£¬¾łŗ¬ÓŠČ©»ł£¬ĖłŅŌ¾łæÉÓėŠĀÖĘCu£ØOH£©2·“Ó¦£¬¹ŹÕżČ·£»
b£®øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOHæÉÓėNaHCO3ČÜŅŗ·“Ӧɜ³ÉĘųÅŻ”¢DĪŖCH3CHO²»ÓėNaHCO3ČÜŅŗ·“Ó¦£¬ĖłŅŌæÉÓĆNaHCO3ČÜŅŗ¼ų±š¶žÕߣ¬¹ŹÕżČ·£»
c£®øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOH”¢DĪŖCH3CHO£¬ŗĖ“Ź²ÕńĒāĘ×ÉĻ¶¼ÓŠ2×éĪüŹÕ·å£¬¹ŹÕżČ·£»
d£®øł¾ŻŅŌÉĻ·ÖĪö£¬BĪŖHCOOH”¢DĪŖCH3CHO£¬¾łŗ¬ÓŠČ©»ł£¬¾łÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬¹ŹÕżČ·£»
¹ŹŃ”£ŗabcd£»
£Ø4£©BÓėEŌŚÅØĮņĖį¼ÓČČĢõ¼žĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉF£¬ŌņBÓėE·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
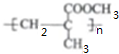
£Ø5£©FĪŖHCOOCH2CH3£¬Ķ¬·ÖŅģ¹¹ĢåG¾ßÓŠĻĀĮŠĢŲµć£ŗ¢ŁÄÜ·¢ÉśŅų¾µ·“Ó¦£¬Ōņŗ¬ÓŠČ©»ł£»¢Ś²»ŗ¬¼×»ł£¬ŌņĮķŅ»øöŃõŌ×ÓÖ»ÄÜŅŌōĒ»łµÄŠĪŹ½Į¬ŌŚÄ©¶ĖµÄĢ¼ÉĻ£¬ĖłŅŌGµÄ½į¹¹¼ņŹ½ĪŖ 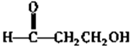 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ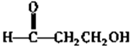 £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲÓŚæ¼²éѧɜ·ÖĪöÄÜĮ¦”¢ĶʶĻÄÜĮ¦ŗĶ×ŪŗĻŌĖÓĆ»ÆѧÖŖŹ¶µÄÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā°ŃĪÕĢāøųŠÅĻ¢£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£®


 ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±Ė®Ź¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£ŗNH3•H2O?NH4++OH- | |
| B£® | ¹¤ŅµÉĻÓĆ¹żĮæµÄNaOHČÜŅŗĪüŹÕ£ŗSO2£ŗSO2+OH-=HSO3- | |
| C£® | ÓĆÉÕ¼īČÜŅŗĒåĻ“ĀĮ±ķĆęµÄŃõ»ÆĤ£ŗ2OH-+Al2O3=2AlO2-+H2O | |
| D£® | ÓĆŹÆ»ŅČéĪüŹÕŠ¹Ā¶µÄĀČĘų£ŗCa£ØOH£©2+Cl2=Ca2++Cl-+ClO-+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓƱ„ŗĶĮņĖįļ§ČÜŅŗ³Įµķµ°°×ÖŹ | |
| B£® | ÓĆÉśŹÆ»ŅøÉŌļ°±Ęų | |
| C£® | ÓĆĀĮÖʵÄČŻĘ÷Ź¢×°ÅØĮņĖį | |
| D£® | ÓƱ„ŗĶĢ¼ĖįÄĘČÜŅŗŹÕ¼ÆŹµŃéŹŅÖĘČ”µÄŅŅĖįŅŅõ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪļÖŹ | æŖŹ¼³Įµķ | ³ĮµķĶźČ« |
| Fe£ØOH£©2 | 7.6 | 9.6 |
| Fe£ØOH£©3 | 2.7 | 3.7 |
| Cu£ØOH£©2 | 4.4 | 8.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
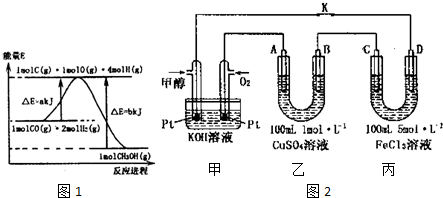
| ĪĀ¶Č\Ź±¼ä | 10min | 20min | 30min | 40min | 50min | 60min |
| 300”ę | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500”ę | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŌŖĖŲ±ąŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą |
| Ō×Ó°ė¾¶/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| ×īøß»ÆŗĻ¼Ū»ņ ×īµĶ»ÆŗĻ¼Ū | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A£® | ŌŖĖŲ¢Ś¢ŽŠĪ³ÉµÄ»ÆŗĻĪļ¾ßÓŠĮ½ŠŌ | |
| B£® | ŌŖĖŲ¢ŚĘųĢ¬Ēā»ÆĪļµÄ·ŠµćŠ”ÓŚŌŖĖŲ¢ŻĘųĢ¬Ēā»ÆĪļµÄ·Šµć | |
| C£® | ŌŖĖŲ¢Ż¶ŌÓ¦µÄĄė×Ó°ė¾¶“óÓŚŌŖĖŲ¢ß¶ŌÓ¦µÄĄė×Ó°ė¾¶ | |
| D£® | ŌŖĖŲ¢ÜµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ±ČŌŖĖŲ¢ŻµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®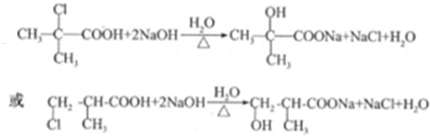 £ØČĪŠ“Ņ»øö£©
£ØČĪŠ“Ņ»øö£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉĪüČėæÅĮ£Īļ£ØPM10£© | B£® | NO2ÅØ¶Č | ||
| C£® | SO2ÅØ¶Č | D£® | CO2ÅØ¶Č |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com