
滴加新制氯水后,下列各组离子可能大量存在的是
A.Fe3+、Cl-、NO3- B.Na+、HCO3-、SO42-
C.Ag+、NH4+、NO3- D.Na+、SO32-、SO42-
科目:高中化学 来源: 题型:
用乙炔为原料制取CH2Br—CHBrCl,可行的反应途径是( )
A.先加Cl2,再加Br2
B.先加Cl2,再加HBr
C.先加HCl,再加HBr
D.先加HCl,再加Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
以石油裂解产物烯烃为原料合成一些新物质的路线如下。
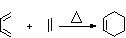 已知:Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的Diels-Alder反应是
已知:Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的Diels-Alder反应是

完成下列填空:
42.写出X分子中所含官能团的名称 。
43.写出A→B的化学方程式 。
44.写出甲物质的名称 。
45.属于酯类且分子中含有两个甲基的Y的同分异构体有 种。
46.R是W的一种同分异构体,R遇FeCl3溶液显紫色,但R不能与浓溴水反应,写出R的结构简式 。
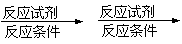 47.写出实验室由D制备E的合成路线。
47.写出实验室由D制备E的合成路线。
(合成路线常用的表示方式为:A B ∙∙∙∙∙∙ 目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的说法正确的是 。
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)〈Ksp(CuS)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质间的每步转化都能通过一步反应实现的是
①Fe→Fe2O3→Fe(OH)3 ② Na→Na2O2→Na2CO3
③ S→SO3→H2SO4→MgSO4 ④ C→CO→CO2→Na2CO3
A.①② B.③④ C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应。
(1)写出反应的化学方程式: 。
(2)生成的氨气在标准状况下的体积是 L。
(3)若将这些氨气溶于水配成500mL氨水,该氨水的物质的量浓度是 mol·L-1。
(4)在400℃左右且有催化剂存在的情况下,用氨可以把一氧化氮还原成氮气,方程式为:4NH3+6NO=5N2+6H2O,此反应中氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
研究发现铜具有独特的杀菌功能,能较好地抑制病菌的生长。工业上铜冶炼大致可分为:
①富集:将硫化物矿石进行浮选;
②焙烧,主要反应为:2CuFeS2+4O2→Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃主要的反应为:2Cu2S+3O2→2Cu2O+2SO2;2Cu2O+Cu2S→6Cu+SO2↑;
④电解精炼,在阴极得到精铜。
下列说法不正确的是
A.上述生产过程中的尾气可以通入氨水中,生产氮肥
B.电解精炼时,粗铜应与外电源的正极相连
C.反应2Cu2O+Cu2S→6Cu+SO2↑中的Cu2O是氧化剂
D.每生产6mol Cu,理论上需消耗11mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,密闭容器中M、N、R三种气体的初始浓度和平衡浓度如下表所示:
| 物质 | M | N | R |
| 初始浓度/mol•L—1 | 0.20 | 0.30 | 0 |
| 平衡浓度/mol•L—1 | 0.02 | 0.21 | 0.18 |
(1)请通过计算写出此反应的化学方程式。
(2)达平衡时,N的转化率是多少?
(3)该温度下的平衡常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com