
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
|
|
|
|
NaCl溶于水 | 铁的吸氧腐蚀原理 | 铜锌原电池构造和原理 | N2与O2反应能量变化 |
NaCl=Na+ + Cl- | 负极:Fe - 2e-=Fe2+ | 总反应:Zn + Cu2+=Zn2+ + Cu | N2(g) + O2(g)=2NO(g)ΔH=-180 kJ·mol-1 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】生产硝酸钙的工业废水常含有 NH4NO3,可用电解法净化。其工作原理如图所 示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的()
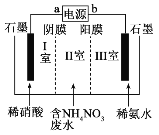
A.a 极为电源正极,b 极为电源负极
B.装置工作时电子由 b 极流出,经导线、电解槽 流入 a 极
C.I 室和 III 室最终均能得到副产品 NH4NO3
D.阴极电极反应式为 2NO3-+12H++10e-==N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家用蘸墨汁书写后的纸张作空气电极(图1),设计并组装出一种轻型、能折叠的可充电锂空气电池,其工作原理如图2所示。下列有关说法正确的是

A.闭合开关K给锂电池充电,X为直流电源负极
B.放电时,纸张中的纤维素作锂电池的正极
C.放电时,Li+由正极经过液相有机电解质移向负极
D.充电时,阳极的电极反应式为Li2O2+2e -=O2↑+2Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和生产中有广泛应用。
(1)用生物质热解气(主要成分为 CO、CH4、H2)将SO2在一定条件下还原为单质硫进行烟 气脱硫。已知:①C(s)+O2(g)=CO2(g)ΔH1= -393.5 kJ·mol-1
②CO2(g)+C(s)=2CO(g) ΔH2= + 172.5 kJ·mol-1
③S(s)+O2(g)=SO2(g) ΔH3= -296.0kJ·mol-1
CO将SO2还原为单质硫的热化学方程式为_______。
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生 反应CO(g)+2H2(g)![]() CH3OH(g),达到平衡后测得各组分的浓度如下:
CH3OH(g),达到平衡后测得各组分的浓度如下:
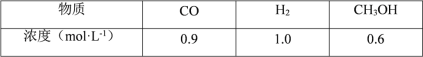
①反应达到平衡时,CO的转化率为_______。
②该反应的平衡常数值 K=_______。
③恒温恒容条件下,可以说明反应已达到平衡状态的是_______(填标号)。
A v 正(CO)=2v 逆(H2) B 混合气体的密度不变
C 混合气体的平均相对分子质量不变 D CH3OH、CO、H2 的浓度都不再发生变化
④若保持容器体积不变,再充入 0.6mol CO 和 0.4mol CH3OH,此时v正_______v逆(填“ >” 、< ”或“= ”)。
(3)在常温下,亚硝酸HNO2的电离常数 Ka=7.1×10-4mol·L-1,NH3·H2O的电离常数 Kb=1.7×10-5mol·L-1。0.1mol·L-1 NH4NO2溶液中离子浓度由大到小的顺序是__________,常温下NO2-水解反应的平衡常数Kh=_______(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某![]() 的X溶液中可能含有
的X溶液中可能含有![]() 、
、![]() ,
,![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法正确的是
中的若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法正确的是![]()
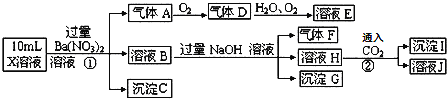
A.气体A是![]()
B.X中肯定存在![]() 、
、![]() 、
、![]() 、
、![]()
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是 ![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,将10 mL a mol·L-1 Na3AsO3、10 mL a mol·L-1 I2和10 mL NaOH溶液混合,发生反应:AsO33-(aq) + I2(aq) + 2OH-(aq)![]() AsO43-(aq) + 2I-(aq) + H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
AsO43-(aq) + 2I-(aq) + H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是

A.溶液的pH不再变化
B.v正(I-)=2v逆(AsO33-)
C.![]() 不再变化
不再变化
D.c(AsO43-)=2b mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学知识在生活中应用广泛。
(1)糖类、油脂和蛋白质是动物性和植物性食物中的基本营养物质。
①下列有关说法中,正确的是________________;
A.棉、麻、木材、蚕丝的主要成分都是纤维素
B.油脂是产生能量最高的营养物质
C.蛋白质在人体内发生水解最终生成氨基酸
D.糖类都是有甜味的物质
E.淀粉、纤维素、蛋白质都是天然高分子化合物
F.硫酸铵或乙酸铅溶液加入到蛋白质溶液中,蛋白质都能从溶液中析出
②葡萄糖是最重要、最简单的单糖,除了是一种营养物质,还能用在制镜等工业上。写出葡萄糖发生银镜反应的化学方程式:_____________________________________________。
(2)苹果酸常用作汽水、糖果的添加剂,其结构简式为![]() ,该分子中官能团的名称为________________,可以和醇类物质发生__________反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为_________________。
,该分子中官能团的名称为________________,可以和醇类物质发生__________反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为_________________。
(3)实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)

①在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_____________;
②生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的有(填序号)___________________;
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的浓度不再变化
③现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。

试剂a是______,分离方法①是_______;分离方法②是________,试剂b是________;
④写出C → D 反应的化学方程式________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2+ O2![]() 2SO3达到平衡的标志是
2SO3达到平衡的标志是
①消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A.①②B.①③C.只有③D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电解乙二醛制备乙二酸(HOOC-COOH)的装置如图所示,通电后,Pt2电极上产生的氯气将乙二醛氧化为乙二酸,下列说法正确的是( )
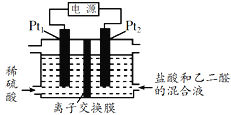
A. Pt2接电源的负极,发生还原反应
B. 电路上每转移1mol电子产生45g乙二酸
C. 盐酸的作用是提供Cl-和增强导电性
D. Pt1极上的电极反应为:2H2O-4e-=== O2↑ + 4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com