
| A. | NaOH溶液洗气时发生反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O | |
| B. | 根据实验可以得出中性条件下,氧化性Cl2>O2 | |
| C. | 根据实验可以得出反应物的浓度和溶液的pH会影响物质的氧化性 | |
| D. | 当电路中通过2mol电子时,阳极可收集到标准状况下气体体积为22.4L |
分析 A.由②用足量NaOH溶液充分洗气,气体体积减少,可知氯气与NaOH反应;
B.由③向酸性的淀粉KI溶液中通入空气,溶液颜色不变,可知氧气不能氧化KI,而①中氯气可氧化KI;
C.由实验①②③可知,浓度不同、酸碱性不同;
D.发生2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,阳极上阴离子放电生成氯气,但氯气与碱反应.
解答 解:A.由②用足量NaOH溶液充分洗气,气体体积减少,可知氯气与NaOH反应,洗气时发生反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故A正确;
B.由③向酸性的淀粉KI溶液中通入空气,溶液颜色不变,可知氧气不能氧化KI,而①中氯气可氧化KI,则中性条件下,氧化性Cl2>O2,故B正确;
C.由实验①②③可知,浓度不同、酸碱性不同,则反应物的浓度和溶液的pH会影响物质的氧化性,故C正确;
D.发生2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,阳极上阴离子放电生成氯气,但氯气与碱反应,则当电路中通过2mol电子时,阳极可收集到标准状况下气体体积小于22.4L,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验操作和技能、电解反应及物质的性质为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①②③④ | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液中:H+、I-、NO3-、SiO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | 饱和CO2溶液中:H+、NH4+、Al3+、SO42- | |
| D. | 加入金属铝产生H2的溶液中:NH4+、Na+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
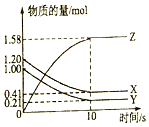 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com