
| A. | 26.3 | B. | 13.2 | C. | 19.8 | D. | 无法计算 |
分析 先根据NH4HCO3分解求出混合气体的平均摩尔质量,然后利用密度之比等于摩尔质量之比计算,以此解答.
解答 解:设NH4HCO3为1mol,由方程式NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑可知,生成NH3、H2O、CO2气体各为1mol,则混合气平均摩尔质量为$\frac{(17+18+44)g}{3mol}$=26.33g/mol,因氢气密度之比等于摩尔质量之比,所以混合气的密度是相同条件下的氢气密度的$\frac{26.33}{2}$=13.2,
故选B.
点评 本题结合铵盐的化学性质,为高频考点,考查了阿伏伽德罗定律推论应用等,有利于培养学生的分析能力和计算能力,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 使用高效催化剂 | B. | 充入更多N2 | C. | 降低温度 | D. | 增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
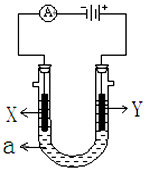 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现象相同,沉淀量相等 | B. | 现象不同,沉淀量不等 | ||
| C. | 现象相同,沉淀量不等 | D. | 现象不同,沉淀量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com