
【题目】用含SO2的硫酸工业尾气联合制备(NH4)2SO4和MnxOy,其工艺流和如下:

(1)反应I的化学方程式为__________;反应II控制温度60℃~70℃之间的原因是________。反应I到反应II的过程中可循环利用的物质是__________________。
(2)反应III中以SO2作___________剂。
(3)MnCO3的作用是除去滤液中的Fe3+,写出除去Fe3+的离子反应方程式___________。
(4)MnS的作用是提供S2-除去Ni2+和Cu2+;当Ni2+恰好完全沉淀时[c(Ni2+)= 1.0×10-5 mol·L -1〕,溶被中Cu2+的浓度是_______ mol·L -1(已知Ksp(CuS)=8.4×10-45, Ksp(NiS)=1.4×10-24,) 。
(5)从MnSO4溶液中获得MnSO4·nH2O的方法是_____________。
(6) “锻烧”时温度与剩余固体质量变化曲线如下图:

该曲线中B点所表示的固体氧化物的化学式为_______________。
【答案】 2SO2+2CaCO3+O2=2CaSO4+2CO2 温度过高NH4HCO3会分解,温度过低反应会较慢 CaCO3 还原 3MnCO3+2Fe3++3H2O=3Mn2++2Fe(OH)3↓+3CO2↑ 6.0×10-26 重结晶 Mn3O4
【解析】(1)根据流程可知,反应I是二氧化硫与碳酸钙和空气反应生成硫酸钙和二氧化碳,其化学方程式为2SO2+2CaCO3+O2=2CaSO4+2CO2;反应II控制温度60℃~70℃之间的原因是温度过高NH4HCO3会分解,温度过低反应会较慢;反应I需要加和碳酸钙,反应II产生碳酸钙,故过程中可循环利用的物质是CaCO3;(2)反应III中SO2转化为硫酸盐,故转化过程被氧化作为还原剂;(3)MnCO3的作用是除去滤液中的Fe3+,将其转化为氢氧化铁的同时产生二氧化碳,故除去Fe3+的离子反应方程式为:3MnCO3+2Fe3++3H2O=3Mn2++2Fe(OH)3↓+3CO2↑;(4)当Ni2+恰好完全沉淀时[c(Ni2+)= 1.0×10-5 mol·L -1〕,MnS的作用是提供c(S2-)=![]() =1.4×10-19 mol·L -1,c(Cu2+)=
=1.4×10-19 mol·L -1,c(Cu2+)=![]() = 6.0×10-26 mol·L -1;(5)从MnSO4溶液中获得MnSO4·nH2O的方法是重结晶;(6)由流程图可知硫酸锰晶体锻烧得到四氧化三锰,根据图中数据,由Mn守恒确认B为四氧化三锰。
= 6.0×10-26 mol·L -1;(5)从MnSO4溶液中获得MnSO4·nH2O的方法是重结晶;(6)由流程图可知硫酸锰晶体锻烧得到四氧化三锰,根据图中数据,由Mn守恒确认B为四氧化三锰。


科目:高中化学 来源: 题型:
【题目】利用下图所示装置一定条件下可实现有机物的电化学储氢(忽略其他有机物)。下列说法不正确的是
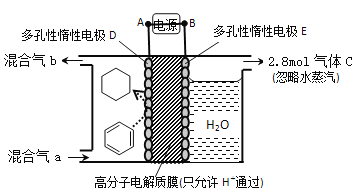
A. A为电源的负极
B. E极的电极式为2H2O-4e-=4H++O2↑
C. D极生成目标产物的电极式为C6H6+6H++6e-=C6H12
D. 该装置的电流效率![]() 75%
75%![]() ,则b中环己烷增加2.8mol
,则b中环己烷增加2.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,恒容密闭容器中发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O)(g),下列叙述不能说明该反应达平衡的是( )
4NO(g)+6H2O)(g),下列叙述不能说明该反应达平衡的是( )
A.V(正)(O2)=![]() V(逆)(NO)B.密闭容器内气体的密度不再改变
V(逆)(NO)B.密闭容器内气体的密度不再改变
C.密闭容器的压强不变D.氮气的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)下列反应属于放热反应的是___
A、铝片与稀H2SO4反应制取H2
B、碳酸钙高温分解成氧化钙和二氧化碳
C、葡萄糖在人体内氧化分解
D、氢氧化钾和硫酸中和
E.Ba(OH)28H2O与NH4Cl固体反应
(2)一定条件下,某恒容密闭容器中充入SO2与O2反应,经5min后,若SO2和SO3物质的量浓度分别为2mol/L和5mol/L,则SO2起始物质的量浓度为___:用SO3表示这段时间该化学反应速率为___,以下操作会引起化学反应速率变快的是___。
A、向容器中通入O2B、扩大容器的体积C、使用正催化剂D、升高温度E.向容器中通入氦气
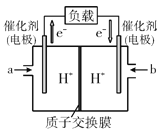
(3)如图是某笔记本电脑使用的甲醇空气燃料电池的结构示意图。放电时甲醇应从___处通入(填“a”或““b“),电池内部H+向___(填“左”或“右”)移动,写出正极的电极反应式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B. 容量瓶、量筒上都标有使用温度,都无“0”刻度,用量筒量取完液体后需洗涤残留在内壁上的液体并与刚量完的液体合并
C. 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
D. 用容量瓶配溶液时,若加水超过刻度线,立即倒掉重配
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述不正确的是
A.适当地摄入一定量的油脂,能促进脂溶性维生素的吸收
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖在人体内发生氧化反应能放出大量热量
D.淀粉、纤维素、油脂、蛋白质都是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是( )

A. H2A为二元弱酸,稀释前c(H2A)=0.005mol/L
B. NaHA水溶液中:c(Na+)+ c(H+)= 2c(A2-)+ c(OH-)
C. 含等物质的量的NaHA、NaHB的混合溶液中:c(Na+)= c(A2-)+ c(B2-)+ c(HB-)+ c(H2B)
D. pH=10的NaHB溶液中,离子浓度大小为:c(Na+)>c(HB-)>c(OH-)>c(B2-)>c(H2B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有H+浓度均为0.1mol/L的醋酸甲和盐酸乙:
(1)请写出醋酸的电离常数的表达式:_____。
(2)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡__________(填“向左”、“向右”或“不”)移动,若加入少量的冰醋酸,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将________(填“增大”、“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,加入足量的金属镁,开始反应时的速率:甲___乙(填“大于”、“小于”或“等于”)。产生氢气的体积:甲___乙(填“大于”、“小于”或“等于”)。
(4)0.1mol/L的甲溶液和0.05mol/L的甲溶液中氢离子浓度:前者是后者的_____。
A.小于2倍 B. 大于2倍 C. 等于2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com