
随着工业的发展,人口增加,引发了许多环境问题。试分析下图,简述硫在自然界的循环过程,并思考人类的行为对硫的循环有什么影响。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、加入明矾,使海水的盐份沉淀并淡化 | B、利用太阳能,将海水蒸馏淡化 | C、将海水通过离子交换树脂,以除去所含的盐分 | D、利用半透膜,采用反渗透法而使海水淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(17分)随着世界工业经济的发展、人口的剧增,全球能源紧缺面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
![]() C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
①该反应的平衡常数表达式为 。
②下列措施中,不能提高碳的转化率的是 (填字母序号)
A.容器的体积不变,增加水蒸气的物质的量 B.缩小容器的体积,增大压强
C.及时将水煤气从容器中移走 D.其他条件不变,升高温度
![]() ③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1
③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1
![]() 则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为 。
则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为 。
![]() (2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图:
(2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图:
①a处通入的是 (填物质名称),该电池工作过程中,H+的移动方向
为从 到 (填“左”或“右”)
②该电池正极反应式为 。
③若用该电池提供的电能电解600ml 0.2mol·L-1NaCl溶液,设有0.01molCH3OH完全放电,且电解产生的Cl2全部溢出,电解前后忽略溶液体积的变化,则电解时阴极反应式为 ,电解结束后所得溶液的pH= 。若向电解后的溶液加入适量的醋酸至溶液的pH恰好等于7(反应前后忽略溶液体积的变化),则此时溶液中c(Na+):c(CH3COO-)= 。
查看答案和解析>>
科目:高中化学 来源:2012届山东省临沂市苍山县高三上学期期末检测化学试卷 题型:填空题
(17分)随着世界工业经济的发展、人口的剧增,全球能源紧缺面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为: C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
①该反应的平衡常数表达式为 。
②下列措施中,不能提高碳的转化率的是 (填字母序号)
| A.容器的体积不变,增加水蒸气的物质的量 | B.缩小容器的体积,增大压强 |
| C.及时将水煤气从容器中移走 | D.其他条件不变,升高温度 |
 ③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1
③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1 则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为 。
则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为 。 (2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图:
(2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图: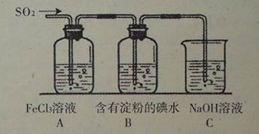
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省临沂市苍山县高三上学期期末检测化学试卷 题型:填空题
(17分)随着世界工业经济的发展、人口的剧增,全球能源紧缺面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
 C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
①该反应的平衡常数表达式为 。
②下列措施中,不能提高碳的转化率的是 (填字母序号)
A.容器的体积不变,增加水蒸气的物质的量 B.缩小容器的体积,增大压强
C.及时将水煤气从容器中移走 D.其他条件不变,升高温度
 ③又知C(s)+CO2(g)
2CO(g) △H=+172.5kJ·mol-1
③又知C(s)+CO2(g)
2CO(g) △H=+172.5kJ·mol-1
 则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为
。
则CO(g)+H2O(g) CO2(g)+H2(g)的焓变(△H)为
。
 (2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图:
(2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g) CH3OH(g)。甲醇作为一种可再生能源燃料,可用于燃料电池。下图是甲醇燃料的原理示意图:
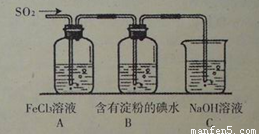
①a处通入的是 (填物质名称),该电池工作过程中,H+的移动方向
为从 到 (填“左”或“右”)
②该电池正极反应式为 。
③若用该电池提供的电能电解600ml 0.2mol·L-1NaCl溶液,设有0.01molCH3OH完全放电,且电解产生的Cl2全部溢出,电解前后忽略溶液体积的变化,则电解时阴极反应式为 ,电解结束后所得溶液的pH= 。若向电解后的溶液加入适量的醋酸至溶液的pH恰好等于7(反应前后忽略溶液体积的变化),则此时溶液中c(Na+):c(CH3COO-)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com