
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |

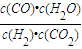 ,
,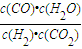 ,
, =
=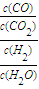 =
=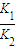 ,
, ;
;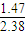 =0.62,1173时K3=
=0.62,1173时K3=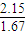 =1.29,则升高温度平衡常数增大,说明升高温度平衡向正反应方向移动,正反应吸热,要使平衡右移,应减少CO的量或升高温度,故选:DF;
=1.29,则升高温度平衡常数增大,说明升高温度平衡向正反应方向移动,正反应吸热,要使平衡右移,应减少CO的量或升高温度,故选:DF;

科目:高中化学 来源: 题型:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| K1 |
| K2 |
| K1 |
| K2 |
| 各物质某一状态时的物质的量浓度/mol?L-1 | ||||||
| c(CO2) | c(H2 ) | c(CO) | c(H2O ) | Qc | 平衡 | |
| ① | 0.004 | 0.004 | 0.006 | 0.006 | 已达平衡 | |
| ② | 0.062 | 0.084 | 0.039 | 0.279 | 2.09 | |
| ③ | 0.182 | 0.086 | 0.098 | 0.359 | 2.25 | |
| ④ | 0.078 | 0.142 | 0.280 | 0.120 | 平衡逆向移动 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
| c(CO)?c(H2O) |
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| c(H2)?c(CO2) |
| K1 |
| K2 |
| K1 |
| K2 |
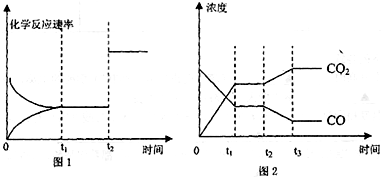
查看答案和解析>>
科目:高中化学 来源: 题型:
 FeO(s)+CO(g) 平衡常数为K1;
FeO(s)+CO(g) 平衡常数为K1; FeO(s)+H2(g) 平衡常数为K2
FeO(s)+H2(g) 平衡常数为K2| 温度/℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
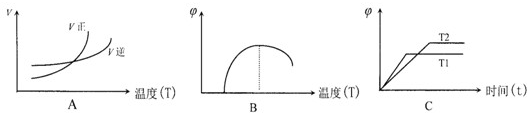
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
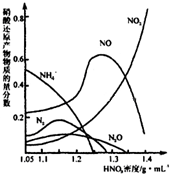
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com